Elektronide konfiguratsioon on elektronide paigutus aatomi sees. Elektronide konfiguratsioon kirjeldab, kus elektronid asuvad orbitaalides. Elementide perioodilisussüsteemi struktuur põhineb osaliselt elektronkonfiguratsioonil.
Elektronkonfiguratsioon seletab, kuidas elektronid jagunevad erinevate energiatsoonide ja alatorude vahel. See mõjutab otseselt aatomi keemilisi omadusi, sh valentsielektronide arvu, ioonide tekkimist, keemilist sidumist ja reaaktiivsust. Konfiguratsioon väljendatakse tavaliselt lühivormis nii, et iga alatoru ja selle elektronide arv on kirjutatud kujul näiteks 1s2 2s2 2p6.
Orbitaalitüübid ja nende maht
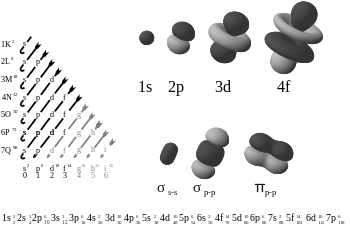
On olemas neli põhilist orbitaalitüüpi: s, p, d ja f.
- s-orbitaal — ligikaudu kerakujuline; ühe s-alatoru maksimaalne elektronide arv on 2.
- p-orbitaal — hantlikujulised kolm alatoru (px, py, pz); kokku mahub p-alatorusse kuni 6 elektroni.
- d-orbitaal — viis alatoru, sageli kompleksse neljalehelise kujuga; d-alatoru mahutab kuni 10 elektroni.
- f-orbitaal — seitse alatoru, keerukamad kujud ja kuni 14 elektroni.
Suured põhimõtted, mis määravad täitumise
- Aufbau-printsiip — elektronid täidavad esmalt madalama energiaga orbitaale enne kõrgema energiaga orbitaalide sattumist (nt 1s enne 2s ja 2p).
- Pauli tõrjeprintsiip — ühes orbitaalis ei saa olla kahte elektroni sama kvantseisundiga; iga orbitaal mahutab maksimaalselt kaks vastassuunalise spiniga elektroni.
- Hundi reegel — samasse alatorusse (näiteks p- või d-alatorusse) asetatakse elektronid esmajoones eri orbitaalides üksikult sama spinniga, alles siis hakatakse paaristama.
Täitumisjärjekord ja erandid
Praktiline täitumisjärjestus (lihtsustatud) on: 1s → 2s → 2p → 3s → 3p → 4s → 3d → 4p → 5s → 4d → 5p → 6s → 4f → 5d → 6p jne. Selle järjestuse põhjuseks on alatorude omavaheline energiahierarhia ja n + l reegel (kus n on peamine kvantarv ja l alatoru kvantarv). Siiski esineb erandeid eriti ülemineku- ja ülemineku-metallide puhul — tuntud näited on kroom (Cr) ja kuper (Cu), mille konfiguratsioonid eristuvad oodatust, kuna pooltäidetud või täidetud d-alatorud annavad täiendavat stabiilsust.
Praktilised näited
- Vesinik (H): 1s1
- Heelium (He): 1s2
- Hapnik (O): 1s2 2s2 2p4 — valentskestal 6 elektroni (2s+2p).
- Raud (Fe): lühendatud konfiguratsioon [Ar] 4s2 3d6 (või analüüsides sageli [Ar] 3d6 4s2), kus [Ar] tähistab heeliumi järgset väärisgaasi tuuma- ja sisekihti.
Lühivorm ja väärisgaasi süntaks
Elektronkonfiguratsiooni kirjutamisel kasutatakse tihti väärisgaasi lühivormi: esmalt kirjutatakse eelnev väärisgaas sulgudes (nt [Ne], [Ar]), mis tähistab sisekihte, ja seejärel lisatakse ülejäänud alatorude konfiguratsioon. See teeb pikkade konfiguratsioonide lugemise lihtsamaks.
Miks see on tähtis
Elektronkonfiguratsioon seletab, miks elemendid sama rühma sees perioodilisustabelis käituvad sarnaselt — neil on sarnane arvu valentsielektrone. See on alus keemiliste sidemete tekkimisele, magnetiliste omaduste (nt paramagnetism vs diamagnetism) ja elektronide ülekande või jagamisele reaktsioonides. Aatomite ja ioonide konfiguratsioonide mõistmine on seega keskne nii keemias kui ka tahkiste ja materjaliteaduses.