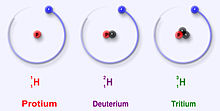
Vesinikul on kolm peamist isotoopi: protium (1H), deuteerium (2H) ja triitium (3H). Need isotoobid esinevad looduses erinevas hulgas. Protium on kõige levinum, deuteerium on stabiilne aga haruldasem ning triitium on radioaktiivne ning selle poolväärtusaeg on ligikaudu 12,3 aastat. Lisaks on laboris toodetud veel raskemaid vesiniku isotoope (näiteks 4H kuni 7H), kuid need on väga ebastabiilsed ja ei esine looduses.
Peamised omadused lühidalt
- Protium (1H): koosneb ühest prootonist ja ei sisalda neutronit. See moodustab suurema osa looduses leiduvast vesinikust ja on keemiliselt aktiivne elementaarne vesinik.
- Deuteerium (2H, D): koosneb ühest prootonist ja ühest neutronist. Massiliselt on deuteerium ligikaudu kaks korda raskem kui protium. Looduslik kontsentratsioon on umbes 0,015–0,02% (u 150–200 ppm). Deuteerium on stabiilne.
- Triitium (3H, T): koosneb ühest prootonist ja kahest neutronist. Triitium on radioaktiivne beeta-emitent ja tekib väikestes kogustes kosmilise kiirguse mõjul või inimtekkelistes protsessides (reaktorid, tuumakatsetused). Selle poolväärtusaeg on umbes 12,3 aastat.
Kasutusalad ja tähtsus
- Protium on tavalise vee ja orgaaniliste ühendite vesiniku vorm ning osaleb kõikides tavapärastes keemilistes reaktsioonides, sealhulgas kütuste (nn vesinikkütus) ja hüdride moodustumisel.
- Deuteerium on oluline teaduslikus ja tööstuslikus kasutuses: deuteeritud vesi (D2O ehk "raske vesi") on neutronite aeglustajana tuumareaktorites, deuteeriumit kasutatakse ka isotopiliseks märgistamiseks orgaanilistes ja bioloogilistes uuringutes ning tuumaspektroskoopias (NMR) eristamiseks protiumist.
- Triitium leiab kasutust tuumaütlemistes (D–T kütus fuusioonikatsetes), radiomärgistajana jälgimisuuringutes ja isesäravate märgistustahvlite/toodete valgustusallikana. Kuna triitium on radioaktiivne, nõuab selle kasutamine ja käitlemine eriluba ja ettevaatusabinõusid.
Tootmine ja levik
Deuteerium tekib peamiselt moodustudes varasema kosmilise protsessi tulemusel ja on looduses stabiilselt olemas merevees. Triitium tekib nii kosmilise kiirguse tagajärjel atmosfääris kui ka tuumareaktsioonide käigus; inimtekkelist triitiumi on tekkinud näiteks tuumakatsetuste ja mõningate reaktoriprotsesside tagajärjel. Tööstuslikult saadakse deuteeriumi ja triitiumi eri meetoditega (distillatsioon, elektrolüüs, neutronikokkupõrgetest tekkiv süntees jms).
Nimede ja sümbolite kasutamine
Vesiniku peamised isotoobid on ainulaadsed selle poolest, et neil on oma nimed. Deuteerium ja triitium tähistatakse sageli lühenditega D ja T, kuid Rahvusvahelisele Puhta ja Rakenduskeemia Liidule (IUPAC) eelistatakse ametlikult tuvastada isotoope numbrilise sümbooliga (näiteks 2H ja 3H). Kuigi D ja T on igapäevases kasutuses mugavad, eelistavad teaduslikud publikatsioonid ja ametlik terminoloogia sageli just numbrilisi kujutisi.
Muud vesiniku isotoobid
Lisaks kolmele peamisele isotoobile on tuvastatud ka raskemad ja üli-raskeid vesiniku isotüüpe (4H kuni 7H). Need tekivad laboritingimustes tuumareaktsioonides ja on äärmiselt ebastabiilsed – nende eluiga on väga lühike (väga väikesed murdosa sekundist), mistõttu neil pole praktilist rolli igapäevases keskkonnas.
Ohutus
Deuteerium ise ei ole radioaktiivne ja ei kujuta erilist radioloogilist ohtu; see on kemikaalina ohutu vastavalt kasutustingimustele. Triitium on madala energia beeta-kiirguse allikas: välist kiirgust on vähe, kuid triitiuminainega segunenud vesi (HTO) võib keha sisse sattudes kujutada sisseimendumisel sisemist radioloogilist ohtu. Sellepärast reguleeritakse triitiumi käitlemist ja käimasolevaid emissioone rangelt.
Kokkuvõtlikult on protium, deuteerium ja triitium vesiniku kolm põhilist isotoopi, mis erinevad neutronite arvus, massis, stabiilsuses ja kasutusalades — alates tavakeemiast kuni tuumatehnoloogia ja teaduslike uuringuteni.