Keemilise elemendi aatomid võivad eksisteerida eri tüüpi. Neid nimetatakse isotoopideks. Neil on sama arv prootoneid (ja elektrone), kuid erinev arv neutroneid. Ühe ja sama elemendi eri isotoopidel on erinevad massid. Mass on suurus, mis väljendab, kui palju ainet milleski on; mass ei sõltu asukohast (vastupidiselt kaalule, mis sõltub gravitatsioonist). Kuna erinevatel isotoopidel on erinev arv neutroneid, ei ole neil kõigil ühesugune mass ega kaal.
Sama elemendi eri isotoopidel on sama aatomiarv — ehk sama arv prootoneid. Aatomiarvu määrab prootonite arv tuumas. Isotoopidel on aga erinev massinumber (nõnda tähistatuna tavaliselt tähe kohal vasakul, nt 12C), sest neil on erinev arv neutroneid.
Sõna „isotoop“ pärineb kreeka keelest ja tähendab „samas kohas“ — see tuleneb asjaolust, et sama elemendi isotoobid paiknevad perioodilisustabelis samal kohal (sest aatomiarv on neil sama), kuigi nende massid erinevad.
Neutraalses aatomis on elektronide arv võrdne prootonite arvuga. Sama elemendi isotoopidel on samuti sama elektronide arv ja seega sama elektroniline struktuur. Kuna aatomi keemilist käitumist määrab peamiselt tema elektronide paigutus, on isotoobid keemiliselt väga sarnased. Füüsikalised omadused (näiteks mass, tihedus, sulamis- ja keemistemperatuur) võivad aga erineda.
Isotoopide tähistus ja näited
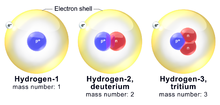
Isotoope tähistatakse tavaliselt elemendi sümboli ja massinumbri abil, näiteks 12C, 13C või 14C (süsiniku isotoobid). Veidi teise vormina kasutatakse ka alaindeksit või kirjutatakse eesruumis (näiteks 14C või 14-C). Tavalisemate vesiniku isotoopide nimed on protium (1H), deuteerium (2H või D) ja tritium (3H) — neist tritium on radioaktiivne.
Massiefekt ja keemilised erinevused
Raskemad isotoobid reageerivad sageli keemiliselt aeglasemalt kui sama elemendi kergemad isotoobid. Seda nähtust nimetatakse massiefektiks või täpsemalt kineetiliseks isotoopmõjuks (kinetic isotope effect). Massiefekt on eriti suur vesiniku ja deuteeriumi vahel, sest deuteeriumi mass on kaks korda suurem kui protiumi mass. Suurema massiga isotoopidel on madalamate sagedustega võnkesid ja erinevad sidemete nullpunktienergiad, mis muudab nende keemiliste reaktsioonide tõenäosust ja kiirust.
Raskemate elementide puhul on erinevused suhtelise aatommassi mõttes väiksemad, seetõttu on massiefekt tavaliselt väike ja keemilised erinevused vähem märgatavad.
Stabiilsus, radioaktiivsus ja looduslik esinemine
Mõned isotoobid on stabiilsed (ei lagune), teised on radioaktiivsed ja lagunevad aja jooksul, saates välja osakesi või kiirgust. Näiteks 14C on radioaktiivne ja seda kasutatakse vanuse määramiseks (radiokarbon-daatimine). Igal elemendil on looduslik segu isotoopidest — see suhteline osakaal ehk loomulik abundantsus määrab ka selle elemendi keskmise aatommassi, mida näidatakse tabelites (nt 12,011 u süsinikul on tingitud 12C ja 13C segust).
Kasutusalad
- Radiokarbon-daatimine (14C) ajalooliste ja arheoloogiliste proovide vanuse määramiseks.
- Mediitsiinis kasutatakse radioaktiivseid isotoope diagnostikas ja ravis (näiteks PET-skaneerimisel või vähiravis).
- Isotoopmärgendamine ja tracer-tehnikad aitavad uurida bioloogilisi ja keemilisi protsesse.
- Tuumaenergeetikas on olulised isotoobid nagu uraan-235 ja plutoonium-239.
- Geokeemias ja paleokliimas kasutatakse isotopivahetusi, et uurida ökosüsteeme ja minevikukliimat.
- Tehases toodetud deuteeritud ühenditega (deuteeritud ravimid) saab muuta aine käitumist metaboolsete radade suhtes.
Isotoopide eraldamine ja mõõtmine
Isotoope saab üksteisest eraldada mitmel viisil: gaasitsentrifuugid (nt uraani isotoopide eraldamiseks), destilleerimine (eriti vesiniku ja vee isotoopide puhul), masspektromeetria abil saab määrata isotoopide suhtelist sisaldust ja täpselt mõõta massinumbreid.
Kokkuvõte
Isotoobid on sama keemilise elemendi aatomid, mis erinevad neutronite arvult ja seetõttu massilt. Nad on keemiliselt väga sarnased, kuna neil on sama elektroniline struktuur, kuid füüsikalised omadused ja reageerimiskiirus võivad massierinevuse tõttu erineda. Isotoopidel on palju praktilisi rakendusi teaduses, meditsiinis ja tööstuses ning nende uurimine aitab mõista nii aatomituuma käitumist kui ka Maa ja elu ajalugu.