Osmoos on vee liikumine läbi poolläbilaskva membraani madala kontsentratsiooniga piirkonnast kõrgema kontsentratsiooniga piirkonda, mille eesmärk on ühtlustada vee kontsentratsioonid ja vähendada lahustunud ainete kontsentratsioonide erinevust. Osmoos on passiivne transport ehk toimib ilma otsese energia (ATP) kasutamiseta. Osmoosisurve tekib seetõttu, et membraani kahel poolel on erinev lahustunud ainete kontsentratsioon, mis tekitab vedeliku liikumise kalduvuse membraani läbilõike suunas.
Kuidas osmoos töötab
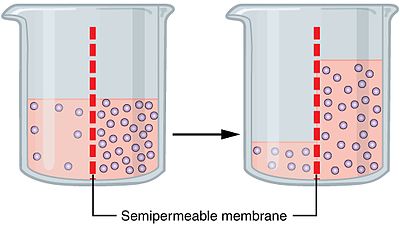
Poolläbilaskv ehk selektiivselt läbilaskev membraan laseb läbi peamiselt lahusti molekule (tavaliselt vee), kuid takistab suuremate või laetud lahustunud osakeste (soolad, suured molekulid) liikumist. Kui ühel pool membraani on rohkem lahustunud aineid, on selle poole vee kontsentratsioon väiksem; vesi liigub siis teiselt poolt membraani, kus on rohkem vaba vett (madalam lahustunud ainete kontsentratsioon), et lahustunud aineid "lahjendada" ja süsteemi tasakaalu suunas liikuda.
Osmoos rakkudes ja orgaanilistes süsteemides
Bioloogias on osmoos eriti oluline rakkude vee- ja ioonitasakaalu säilitamisel. Näited:
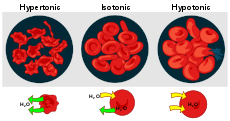
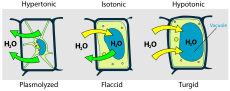
- Kui rakk asetatakse hüpertoonilisse keskkonda (lahus, mille lahustunud ainete kontsentratsioon on rakust suurem), liigub rakkudest välja vesi ja rakk võib kokku tõmbuda (plasmolüüs taimedes või kurrumine loomsetes rakkudes).
- Hüpotoonilises keskkonnas (lahuse kontsentratsioon väiksem kui raku sees) imbub rakku vesi, mis võib tekitada rakkudes rõhku (turgor), eriti olulist taimerakkudes.
- Isotooniline keskkond tähendab, et rakk ja väliskeskkond on osmootiliselt võrdsed — netovett liikumist praktiliselt ei toimu.
Mõõtmine ja osmoosirõhk
Osmoosirõhk (π) on teoreetiline rõhk, mida tuleks rakendada lahuse poole, et takistada osmoosi ehk vee voolu läbi membraani. Lihtsas lahendis järgib osmoosirõhk ligikaudset van’t Hoff’i seadust:
π = i · C · R · T
kõnealuses valemis tähistab C molaarset kontsentratsiooni, R on gaasikonstant, T on absoluuttemperatuur ja i on van’t Hoff’i faktor (näitab, kui palju osakesi aine lahustudes dissotsieerub). See valem kehtib eelkõige lahjades ideaalsetes lahustes.
Faktorid, mis mõjutavad osmoosi kiirust
- Membraani läbilaskvus (poride suurus ja tihedus)
- Pindala — suurem membraani pindala suurendab voolu
- Kontsentratsiooni gradient — suurem erinevus kiirendab osmoosi
- Temperatuur — kõrgem temperatuur suurendab molekulide liikumist ja kiirendab osmoosi
- Rõhk, mis rakendub lahuse poolelt (nt osmoosile vastupidine surve vähendab või peatab vee liikumise)
Tehnilised ja praktilised rakendused
- Pöördsoolamise (reverse osmosis) protsess: rakendades survet lahusele, surutakse vesi membraani kaudu vastupidises suunas, eemaldades sooli ja muid lisandeid — laialt kasutusel joogivee desalinatsioonis ja vee puhastamises.
- Toidutööstus: niiskuse eemaldamine, kontsentreerimine ja steriliseerimine teatud protsessides.
- Meditsiin: dialüüs ja teised biotehnoloogilised protseduurid, kus selektiivne difusioon ja osmoos aitavad eraldada aineid.
- Põllumajandus ja botaanika: taime veetasakaal, kastmise mõju juurtele ja soolastumine mullas.
Kokkuvõte
Osmoos on põhiline füüsikaline protsess, mille kaudu vee liikumine läbi poolläbilaskva membraani püüab vähendada lahustunud ainete kontsentratsiooni erinevusi. See on eluliselt tähtis rakkude homöostaasis ning omab olulisi rakendusi nii tehnikas (nt pöördsoolamine) kui ka igapäevaelus. Mõistmine, kuidas osmoosirõhk ja membraani omadused mõjutavad protsessi, aitab seletada mitmeid bioloogilisi nähtusi ja disainida tõhusaid filtratsioonisüsteeme.
Osmoosi rolli rakkude funktsioonis ja tehnilistes lahendustes saab illustreerida paljude eksperimentide ja näidetega — alates lihtsast suhkru-lahuseampulli lammutamisest kuni tööstusliku veepuhastusjaamani.
Osmoosi ja raku transporti puudutavad täpsemad biokeemilised ja füüsikalised detailid on kirjeldatud laiemalt biokeemia ja füsioloogia õpikutes.