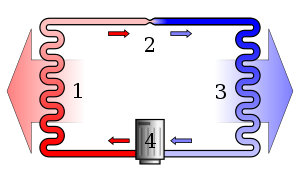
Termodünaamika teine seadus ütleb, et kui energia muutub ühest vormist teise või aine liigub vabalt, suureneb suletud süsteemis entroopia (korrastamatus). See tähendab praktiliselt, et suletud (isoleeritud) süsteemis toimuvad protsessid kulgevad selliselt, et üldine järjestus väheneb ja juhuslikkus suureneb — süsteemi mikrostaatide arv, mis vastab makrostaatile, kipub aja jooksul kasvama.
Temperatuuri, rõhu ja tiheduse erinevused kipuvad mõne aja pärast horisontaalselt tasanduma. Gravitatsioonijõu tõttu ei tasandu tihedus ja rõhk vertikaalselt: tihedus ja rõhk on allpool suuremad kui ülevalpool. See on näide sellest, et termodünaamilised tasakaalutingimused sõltuvad ka välistest jõududest ja piirtingimustest.
Mis on entroopia?
Entroopia on energia ja aine leviku mõõt — laiemal, statistilisel tasandil öeldes on see makrostaatile vastavate mikrostaatide arvu logaritm. Boltzmanni valemina: S = k ln Ω, kus S on entroopia, k on Boltzmanni konstant ja Ω on võimalike mikrostaatide arv. Entroopia kui olekufunktsiooni muutus seostub ka soojusvahetusega: diferentiaalvormis kehtib kadudeta (reversiivse) protsessi puhul dS = δQ_rev / T.
Clausius’i ja Kelvini sõnastused
Termodünaamika teise seaduse tuntuim sõnastus pärineb Rudolf Clausiusest ja seda võib väljendada mitmel ekvivalentsel moel. Originaaltekstist lähtuv lihtsustav väide on, et soojus ei lähe iseenesest külmemast kehast kuumemasse.
Soojus ei saa iseenesest liikuda külmemast kehast kuumemasse.
Lord Kelvini samaväärne avaldus on järgnev:
Ümberkujundamine, mille ainus lõpptulemus on konstantsel temperatuuril allikast võetud soojuse muundamine tööks, on võimatu.
Need kaks väidet (Clausius ja Kelvin–Planck) on formaalselt ekvivalentsed: mõlemad piiravad soojuse ja töö vahelisi pööratavaid teisendusi ning seavad piirid soojusmootorite (näiteks Carnot’ masina) efektiivsusele. Carnot' teoreemi järgi on kõrgeima võimalik efektiivsuse piiriline väärtus kahe termilise reservuaari vahel: η_max = 1 − T_külm / T_soe (temperatuurid absoluutväärtustes).
Matemaatiline ja statistiline tõlgendus
Isolatsioonitingimustes kehtib lihtne ja oluline seos:
- dS_tot ≥ 0 — kogu (süsteemi + keskkonna) entroopia ei lange (võrdus 0 ainult ideaalselt reversiivsete protsesside korral);
- dS = δQ_rev / T — entroopia muutus pööratavas protsessis.
Statistilisest vaatenurgast on teine seadus tõenäosuslik: makroskoopses süsteemis domineerivad mikrostaatid, mis annavad suurema Ω, seega on selliste makrostaatide esinemine tõenäolisem. Väikestes süsteemides võivad tekkida ajutised entroopiale vastupidised kõikumised (joskus nimetatakse neid Fluktuatsiooniteoreemide mõjul), kuid suure hulga osakeste korral on mõju ebaoluline ja teine seadus praktiliselt täiuslik.
Praktilised tagajärjed ja näited
Teisest seadusest tulenevad mitmed tuntud nähtused ja piirangud:
- Soojuse loomulik vool on soojemalt külmemale; selle tõttu ei toimi soojusmootorid 100% efektiivsusega.
- Segunemine (näiteks kaks erineva soojusega veeportsjonit segunevad) on pöördumatu ilma välise töö tegemiseta — entroopia suureneb.
- Elusüsteemid võivad lokaalselt entroopiat vähendada (näiteks teha korda ja ehitada keerukaid struktuure), kuid see nõuab energiat ja põhjustab suurema entroopia kasvu keskkonnas — teine seadus jääb kehtima kogusüsteemi tasandil.
Piirangud ja erandlikud mõisted
Oluline on meeles pidada, et teine seadus kehtib selgelt ja vahetult suurtele, makroskoopilistele ja mitte-kvantmehaanilistele süsteemidele ning käsitleb tõenäolist käitumist. See ei ole absoluutne keel seoses üksikute mikroskoopiliste sündmustega — kvant- ja statistilises füüsikas võivad olla lühiajalised fluktuatsioonid, kus entroopia väheneb, kuid need on ebatõenäolised suures skaalas. Samuti ei tähenda teine seadus, et mingit konkreetset lokaalset entroopia vähendamist ei saa saavutada: seda saab, kuid hinnaks on suurem entroopia kasv mujal (näiteks soojuse eraldumine).
Läheduses olevad teemad
Teise seaduse käsitluses on tihedalt seotud teemad nagu töö ja soojuse vahe, Carnot-tsüklid, irreversiivsus, informatsiooniteooria seosed (näiteks Maxwelli deemon ja Landaueri printsiip, mis näitab informatsiooni töötlemise entroopilist kulu) ning statistiline mehaanikaga tuletatud entroopia mõiste. Kõik need laiendavad arusaama sellest, miks protsessid kulgevad teatud suunas ja millised on praktilised piirid energia muundamisele.
Teine seadus ei ole ainult abstraktne printsiip: see määrab paljude tehnoloogiate (soojusmootorid, külmutusseadmed, elektrijaamad) piirid ning seletab, miks aja jooksul süsteemid püsivalt kipuvad jõudma tasakaaluolekusse, kus temperatuuri- ja rõhuerinevused on likvideeritud või püsivad ainult väliste jõudude (nt gravitatsiooni) mõjul.