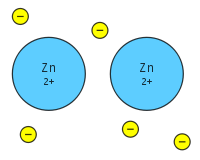
Metalliline side on side, kus paljude eraldunud elektronide jagamine paljudega positiivsete ioonidega loob tugeva, kolmemõõtmelise kristallstruktuuri. Delokaliseerunud elektronide pilv — sageli kirjeldatud kui elektronide "meri" — toimib osaliselt kui "liim", mis hoiab positiivseid metallioone koos. See on oluliselt erinev nii ioonsete sidemete kui ka kovalentsete sidemete loogikast ning annab metallidele iseloomulikke füüsikalisi omadusi.
Valentselektronide roll ja energia
Metallidel on sageli madal ionisatsioonienergia, mistõttu nende väliskihis olevad elektronid ei ole tugevalt seotud üksiku aatomiga ja võivad delokaliseeruda kogu tahke aine ulatuses. Metalli aatomite välised energiatasemed (aatomiorbitaalid) kattuvad ja ühinevad, mille tulemuseks on pidev energiabandide süsteem. Selle tõttu ei ole kõik valentselektronid kinnitatud üksikutele lähimatele naaberaatomitele, vaid kuuluvad ühise elektronide süsteemi.
Omadused, mida metalliline side põhjustab
Metallsidemed annavad metallidele mitmeid iseloomulikke tunnuseid:
- Elektrijuhtivus: delokaliseerunud elektronid liiguvad suhteliselt vabalt, mis võimaldab tekkida elektrivoolul ja annab metallidele kõrge elektrijuhtivuse.
- Soojajuhtivus: vabad elektronid kannavad soojusenergiat efektiivselt läbi struktuuri, mistõttu paljud metallid juhivad soojust hästi (soojus- ja elektrijuhtivus on tihti seotud).
- Mehaanilised omadused: tugev tõmbejõud elektronide ja positiivsete ioonide vahel annab metallidele sageli kõrge tugevuse. Samal ajal võimaldab elektronide delokaliseerumine aatomite libisemist ilma sidemeid murdmata, mis annab metallidele plastilisuse ja (sageli) suure venivuse — samast terminist on originaalis ka teine link plastilisus, mis rõhutab selle omaduse tähtsust.
- Läige: delokaliseerunud elektronid neelavad ja kiirgavad valgust efektiivselt, põhjustades paljude metallide iseloomuliku läike.
Juhtivus ja selle piirangud
Kuna elektronid võivad liikuda kogu kristallis, on metallil teatav elektrijuhtivus. Juhtivus sõltub otseselt elektronide kontsentratsioonist ja nende liikumise takistusest (hajumine fononite, defektide ja lisandite poolt). Seetõttu mõjutavad temperatuur, puhtus ja mikrostruktuur metalli osooniliselt: kõrge temperatuur suurendab elektronide hajumist ja seetõttu suureneb takistus (vähendab juhtivust). On ka mittemetallseid aineid, mis juhivad elektrit — näiteks grafiit, kus on samuti delokaliseerunud elektronid, ning ioonühendid, mis juhivad ainult siis, kui on sulas või lahuses, kuna siis liiguvad laengukandjatena ioonid.
Erandid ja erijuhtumid
Kuigi metalliline side esineb paljudel metallidel, ei ole see universaalne kõikide metalliliste ühendite puhul. Näiteks elavhõbeda ioonid (Hg2+)
2) võivad moodustada kovalentseid metall‑metall sidemeid, mis erinevad traditsioonilisest delokaliseerunud elektronide mehhanismist. Samuti sõltuvad paljud omadused sulamite (nt Sulam) koostisest: sulamid kombineerivad eri metallide omadusi ja võivad olla tugevamad, kõvemad või korrosioonikindlamad kui puhtad metallid.
Põhimõtted kvantmehaanilisest vaatenurgast
Metallilise sideme mõistmiseks on kasulik vaadata energia‑ ja elektronide jaotust bänditeooria kaudu: eraldi aatomiorbitaalidest tekivad moodustamisel molekul‑ või kristallibandid, kus osaliselt täidetud valentsid lubavad elektronidel liikuda. See selgitab palju metalli optilisi ja elektrilisi omadusi ning miks mõned metallid on paremad juhtijad (nt hõbe, vask) kui teised (nt ränidioksiidid, mis on pooljuhid või isoleerijad vastavalt bändide konfiguratsioonile).
Rakendused ja kokkuvõte
Metalliline side on aluseks paljudele tehnoloogiatele: juhtmete ja elektrikomponentide tootmine, soojusvahetid, mehaanilised konstruktsioonid, ehted ja peegeldavad pinnad. Selle varasema kirjeldused — delokaliseerunud elektronide „meri“, madal ionisatsioonienergia ja kattuvad aatomiorbitaalid — aitavad mõista, miks metallid omavad iseloomulikke omadusi nagu elektrijuhtivus, soojusjuhtivus, läige ja plastilisus. Sulamid (Sulam) võimaldavad neid omadusi reguleerida vastavalt vajadusele ja luua uusi materjale igapäevaseks ning tehnikaliseks kasutamiseks.