Väärisgaasid – definitsioon, omadused ja näited
Väärisgaasid: põhjalik ülevaade definitsioonist, omadustest ja näidetest (heelium, neoon, argoon, krypton, xenon, radoon) — huvitavad faktid ja rakendused.
Väärisgaasid on elementide rühm, mis esinevad looduses peaaegu alati gaasilises olekus. Need elemendid kuuluvad perioodilisustabelis 18. rühma ja on üldjuhul üheaatomilised – iga molekul koosneb ühe aatomi ühest üksusest. Väärisgaasid on tuntud oma vähenõudliku keemiaga: nad ei reageeri teiste elementidega kergesti, sest neil on täisväärtuslik väliskest. Erandiks on heelium, mille täisväliskest koosneb 2 elektronist; teistel (neoonist alates) on väliskestal tavaliselt 8 elektroniga elektronkonfiguratsioon.
Esinemine atmosfääris ja allikad
Väärisgaase leidub atmosfääris kokku väikeses koguses – peamiselt moodustab neist õhust umbes 0,94% (enamjaolt argoon). Muud väärisgaasid esinevad atmosfääris vaid mikro- või mõne ppm (miljoniosa) tasemel. Radoon on erand: see on radioaktiivne laguprodukt, mis tekib maa-alustes kivimites ja mullas leiduvatest raskematest radioaktiivsetest elementidest ning võib lokaalselt kontsentratsioonilt suureneda hoonete siseõhus.
Aatomistruktuur ja keemilised omadused
Väärisgaaside vähene keemiline aktiivsus tuleneb nende täistatud valentselektroonidest, mistõttu neil puudub loomulik vajadus elektrone juurde võtta või anda. Traditsiooniliselt peeti neid inertseteks, kuid alates 1960. aastatest on leitud ja sünteesitud mitmeid väärisgaaside ühendeid, eelkõige fluori ja hapniku väga tugeva oksüdeerivuse tingimustes. Näiteid:
- ksenooni fluoriühendid (näiteks XeF2, XeF4, XeF6) ja oksüdeeritud ühendid;
- kriitilisemates tingimustes on saadud kryptoni ühendeid (nt KrF2);
- arooni ühendeid on valmistatud väga äärmuslikes tingimustes (näiteks HArF jäi matrix-konditsioonidesse eksperimentaalselt tuvastatuks);
- heelium ja neoon moodustavad tavalistes tingimustes väga vähe või praktiliselt mitte stabiilseid ühendeid.
Keemiliste sidemete tekkeks on sageli vajalikud tugevad oksüdeerijad, kõrgsurvetemperatuur või madalad temperatuurid ja spetsiifilised katalüütilised tingimused.
Füüsikalised omadused
Väärisgaasid on toatemperatuuril gaasilised, neil on madalad sulamis- ja keemispunktid (heeliumil kõige madalamad), ning erinevad tihedused ja optilised omadused. Heelium on äärmiselt kerge ja omab madalat aurustumisenergiat, seetõttu kasutatakse seda külmutamisel (näiteks MRI magnetite ja teiste cryogeenide jahutamisel). Neoon tekitab elektrilennul punaka-oranži valgust, argoon sinaka-lilla, krüpton ja ksenoon annavad valge kuni sinaka valguse – neid omadusi kasutatakse valgusallikates ja reklaamivalguses.
Rakendused
- Heelium: jahutus (lihtsaima vedeliku saavutamiseks), sukeldumisgaaside segudes (vähendab lämmastikumürgistuse ohtu), õhupallid ja dirigeerid, inertne keskkond keemilistes protsessides.
- Neoon: valgusreklaamid (neonvalgustid) ja kõrgepingeseadmete indikaatorid.
- Argon: ebareaktiivne kaitsegaas keevitamisel ja metallide töötlemisel, lambipirnide täitematerjal, laboratoorsed inertsed tingimused.
- Krüpton ja ksenoon: spetsiaalsed lambid, välgulambid, meditsiinilised seadmed (nt ksenoon-laserid), uurimistöös ja optikas.
- Radoon: peamiselt uurimistöö objekt radioaktiivsuse ja geoloogiliste protsesside puhul; ei sobi üldiseks rakenduseks terviseohtude tõttu.
Tervis ja ohutus
Radoon on radioaktiivne ja pikaajaline kokkupuude suurendab kopsuvähi riski; kõrge radooni tase siseõhus on oluline terviseprobleem ning seetõttu soovitatakse kontrollida ja vajadusel ruumide ventilatsiooni ja muid leevendusmeetmeid rakendada. Ülejäänud väärisgaasid on keemiliselt suhteliselt inertsed ja ebamürgised, kuid surumis- ja lämbumisohtu (suurtes kontsentratsioonides võivad asendada hapniku õhus) ei tohi alahinnata – eriti suletud ruumides ja tööstuslikes tingimustes.
Värvused kõrgepingetorudes
Kui väärisgaase kasutatakse külma katoodiga torudes valguse tekitamiseks, annab iga gaas erineva värvitooni: neoon on punakas-oranž, heelium hele kollakas, argoon sinaka-lilla, krüpton valge-hallikas ja ksenoon sinakas-valge. Kuna radoon on radioaktiivne, ei kasutata seda tavaliselt valgustamiseks. Siin on pildid, kuidas teised välja näevad:
· 
Heelium
· 
Neon
· 
Argoon
· 
Krypton
· 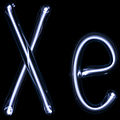
Xenon
Ülesjärglane (element 118)
Ununoctium (element 118) on olnud selle rühma järgne kandidaat. Selle isotoopide poolväärtusaeg on väga lühike (nt on mõõdetud väärtusi ligikaudu 0,89 ms), mistõttu on selle uurimine keeruline ja praktiline kasutus piiratud. Tänapäeval on element 118 ametlik nimetus oganesson (Og), kuid isotoopide kiire lagunemine ja tugevad relativistlikud efektid muudavad selle keemilised omadused raskesti ennustatavaks — mõned teoreetilised mudelid viitavad sellele, et oganesson võiks käituda teistest väärisgaasidest erinedes.
Avastus ja ajalooline taust
Väärisgaaside eraldamise ja uurimise etapi pioneerideks olid lord Rayleigh ja Sir William Ramsay. Nad eraldasid ja identifitseerisid varem tuntud gaaside kõrval uued inertsed gaasid ning uurisid nende omadusi. Mõlemad teadlased pälvisid 1904. aastal Nobeli auhinna: Rayleigh sai Nobeli füüsikapreemia ja Ramsay Nobeli keemiapreemia oma töö eest väärisgaaside alal.
Kokkuvõtlikult on väärisgaasid erilise tähtsusega nii teaduses kui tehnoloogias: nende inertsus, madalad külmumis- ja keemispunktid ning elektriliselt eristatavad luminestsents-omadused annavad neile palju praktilisi kasutusvõimalusi, samas tuleb arvestada mõnede liikide (näiteks radooni) tervise- ja ohutusriske.
Küsimused ja vastused
K: Mis on väärisgaasid?
V: Väärisgaasid on elementide rühm, mis on kõik gaasid ja asuvad perioodilisustabelis 18. rühmas. Neil on täis 8 elektroni välise elektronkesta, mis tähendab, et iga molekul on üks aatom ja nad peaaegu kunagi ei reageeri teiste elementidega.
K: Kui palju on väärisgaase?
V: On kuus väärisgaasi - heelium, neoon, argoon, krüptoon, ksenoon ja radoon.
K: Kus neid väärisgaase leidub?
V: Neid väärisgaase leidub õhus ja need moodustavad umbes 0,96% atmosfäärist.
K: Kas väärisgaasidest saab moodustada ühendeid?
V: Jah, väärisgaasidest võib moodustada ühendeid.
K: Mis juhtub, kui väärisgaasi kasutatakse külma katoodtorudes valguse tootmiseks?
V: Kui väärisgaasi kasutatakse külmkatooditorudes valguse tootmiseks, siis on neil kõigil erinev värvus.
Radooni ei kasutata tavaliselt valgustamiseks, sest see on radioaktiivne.
K: Kes avastas väärisgaasid?
V: Nobelgaasid avastasid Lord Rayleigh ja Sir William Ramsay, kes mõlemad said nendega seotud tööde eest Nobeli preemia - Rayleigh sai Nobeli füüsikapreemia 1904. aastal ja Ramsay Nobeli keemiapreemia samuti 1904. aastal.
Küsimus: Milline element järgneb perioodilisussüsteemi 18. rühma kuuluvale radoonile?
V: Oganesson (element 118) järgneb perioodilisussüsteemi 18. rühma osana radoonile, kuid selle poolväärtusaeg on 0,89 ms, mille järel ta laguneb liivermooriks (element 116), seega on selle kasutamine tõenäoliselt piiratud.
Otsige