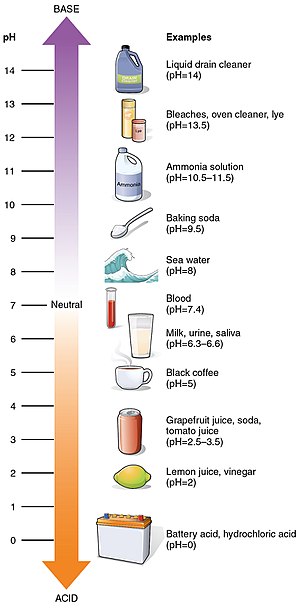
pH on happesuse skaala, mille tavaline ulatus on 0–14. See näitab, kui happeline või leeliseline on lahus: happelisemate lahuste pH on madalam ja leeliseliste lahuste pH kõrgem. Ainetel, mis ei ole happelised ega leeliselised (st neutraalsed lahused), on tavaliselt pH umbes 7. Hapete pH on väiksem kui 7 ja leeliseliste pH on suurem kui 7.
Mis pH tegelikult mõõdab
pH näitab lahuses olevate prootonite (H+) või hüdroniumioonide (H3O+) aktiivsust. Mõiste võttis kasutusele S.P.L. Sørensen 1909. aastal; täht P pärineb saksa keele sõnast potenz (võimsus või kontsentratsioon) ja H tähistab vesinikiooni (H+).
Kuidas pH arvutatakse
Kõige levinum valem pH arvutamiseks on:
pH = - log 10 [ H + ] {\displaystyle {\mbox{pH}}=-\log _{10}\left[{\mbox{H}}^{+}\right]}
[H+] näitab H+ ioonide kontsentratsiooni (kirjutatakse ka [H3O+], mis on võrdne hüdroniumioonide kontsentratsiooniga), mõõdetuna moolides liitri kohta (tuntud ka kui molaarsus).
Tegelikult on aga õigem kasutada iooni aktiivsust:
pH = - log 10 [ a H + ] {\displaystyle {\mbox{pH}}=-\log _{10}\left[a_{\mathrm {H^{+}} }\right]}
kus a H + {\displaystyle a_\mathrm {H^{+}} }
Mida pH-ühikud tähendavad
- pH ühe ühiku muutus vastab H+ kontsentratsiooni kümnekordsele muutusele (nt pH 3 on 10 korda happelisem kui pH 4 ja 100 korda happelisem kui pH 5).
- Paljude ainete pH jääb tüüpiliselt vahemikku 0–14, kuid väga kontsentreeritud happed või alused võivad anda pH < 0 või pH > 14.
- Leeliselistes lahustes domineerivad hüdroksiidioonid (OH−), mille kontsentratsioon on suhteliselt suur.
Seosed teiste suurustega
Vee ioonprodukt (Kw) määrab seose pH ja pOH vahel: pH + pOH = pKw. Tavatingimustel (25 °C) on pKw ≈ 14, seega pH + pOH ≈ 14. Kuid pKw ja seega ka see seos sõltuvad temperatuurist.
Mõõtmine ja praktiline kasutus
pH-i saab määrata mitmel viisil:
- pH-paber või indikaatorkeel (värvimuutus vastavalt pH-le) – lihtne ja odav, sobib ligikaudseks hindamiseks.
- pH-meeter (klaaselektrood + referentselektrood) – täpne mõõtmine, vajab regulaarset kalibreerimist (tavaliselt kalibreeritakse pH 4, 7 ja 10 standardlahustega).
- värviindikaatorid (näiteks fenoolftaleiin) laborikatsetes või biokeemias.
Oluline on arvestada, et pH-mõõtmine võib sõltuda temperatuurist, ioonide tugevusest (ioonitugevusest) ja mõõtmise tingimustest, mistõttu täpsed kvantitatiivsed analüüsid kasutavad tihti aktiivsusi või sobivaid korrigeerimisi.
Praktilised näited ja tähtsus
- Puhas vesi: pH ≈ 7 (neutraalne).
- Värske inimveri: pH ≈ 7,35–7,45 (väga range reguleerimine organismis on eluliselt oluline).
- Hapud toidud: sidrunimahl ~ pH 2, äädikas ~ pH 2,5–3.
- Magnetopõletid ja kodukeemia: valgendid ja ammoniaak võivad olla pH 11–13; tugevad leelised (näiteks naatriumhüdroksiid) võivad saavutada pH 14.
- Mõned kontsentreeritud happed (nt tugev väävel- või kloriidhape) võivad teatud tingimustel anda pH alla 0.
pH on oluline paljudes valdkondades: keemia, bioloogia, meditsiin, veekvaliteedi jälgimine, põllumajandus, toiduainetööstus ja palju muud. Näiteks ensüümide aktiivsus ja taimerakkude toitainete omastamine sõltuvad tugevalt pH-st.
Muud mõisted
Buffersüsteemid (stabilisaatorid) aitavad hoida lahuse pH-d suhteliselt muutumatuna, kui lisatakse väikseid koguseid happet või alust — see on eriti oluline organismides ja biokeemilistes protsessides.
Kokkuvõte: pH on logaritmiline mõõt, mis kirjeldab lahuse vesinikioonide aktiivsust; pH 7 on neutraalne, pH < 7 happeline ja pH > 7 leeliseline. Mõõtmine ja tõlgendamine nõuavad tähelepanu kontsentratsioonile, aktiivsusele ja temperatuurile.
Leeliselistes ainetes on vesinikuioonide asemel hüdroksiidioonide (OH-) kontsentratsioon suurem.
![{\displaystyle {\mbox{pH}}=-\log _{10}\left[{\mbox{H}}^{+}\right]}](https://www.alegsaonline.com/image/093977a79b6a17e02db4699475930e48c05d6468.svg)
![{\displaystyle {\mbox{pH}}=-\log _{10}\left[a_{\mathrm {H^{+}} }\right]}](https://www.alegsaonline.com/image/7a631c4037415f3d4483a6cb07e69858b64890fc.svg)