Keemias on van der Waalsi jõud üks molekulidevaheliste jõudude liik. Molekulidevaheline jõud on suhteliselt nõrk jõud, mis hoiab molekule koos. Van der Waalsi jõud on kõige nõrgemat tüüpi molekulidevahelised jõud. Need on nimetatud Hollandi teadlase Johannes Diderik van der Waalsi (1837-1923) järgi.
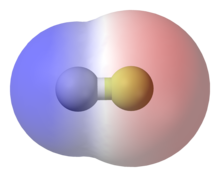
Negatiivselt laetud elektronid tiirlevad molekulide või ioonide ümber. Elektronid tekitavad molekuli ühest otsast teise veidi erinevaid laenguid. Neid väikeseid erinevusi nimetatakse osalisteks laenguteks, nagu δ- või δ+.
Mõnikord kasutatakse seda terminit vabalt kõigi molekulidevaheliste jõudude sünonüümina. Van der Waalsi jõud on kovalentsete sidemetega võrreldes suhteliselt nõrgad, kuid mängivad olulist rolli supramolekulaarses keemias, ensüümides, polümeeriteaduses, nanotehnoloogias, pinnateaduses ja kondenseeritud aine füüsikas. Van der Waalsi jõud määravad paljud orgaaniliste ühendite omadused, sealhulgas nende lahustuvus.
Tüübid ja olemus
- Londoni dispersioonijõud (indutseeritud dipoolid) — universaalsed, tekivad kasvu tõttu elektronide pilve kõikumisest; esinevad kõigi aatomite ja molekulide vahel, eriti olulised mittespolarsete ja suuremate molekulide puhul.
- Dipool–dipool jõud (Keesomi jõud) — tekivad püsivate dipoolidega molekulide vahel, kus osaliste laengute (δ+/δ−) vastastikune orientatsioon põhjustab atraaktiivset tõmmet.
- Dipool–indutseeritud dipool (Debye jõud) — tekivad siis, kui püsiva dipooliga molekul indutseerib dipooli läheduses asuvas molekulis.
- Vesiniksidemed — tihti käsitletakse neid eraldi, sest need on tavapärastest van der Waalsi jõududest tugevamad; tekivad siis, kui H on kovalentselt seotud tugevalt elektronegatiivse aatomiga (näiteks O, N, F) ja tõmbub teise elektronegatiivse aatomi poole.
Matemaatiline kirjeldus ja kaugussõltuvus
Paljusid van der Waalsi komponente kirjeldatakse potentsiaalina, mis langeb kiiresti kaugusega. Näiteks dispersioonijõudude energia sõltub ligikaudu kauguse kuubiku ruudust (sageli esitatakse lihtsustatult kui E ≈ −C / r^6). Praktikas kasutatakse molekulidevaheliste interaktsioonide modelleerimiseks sageli Lennard‑Jonesi potentsiaali (nn 12‑6 potentsiaal), kus üks liige kirjeldab lühikest vahelist tõrjet ja teine jõudvat atraaktsiooni (r^-6).
Mõõtmed ja tegurid, mis mõjutavad tugevust
- Polariseeruvus: suurema elektronpilvega aatomid/molekulid on polariseeruvamad ja annavad tugevamaid dispersioonijõude.
- Molekulide suurus ja mass: suuremad ning raskemad molekulid näitavad tavaliselt kõrgemaid van der Waalsi interaktsioonide energiaid.
- Kuju ja kontaktpind: tasapinnalised või laiad pinnad saavad rohkem ainuühikutest summutatud atraaktiivseid kontakte — jõud on additiivsed ja võivad makroskoopiliselt märkimisväärseks muutuda.
- Keskkond ja temperatuur: kõrgem temperatuur vähendab järjestunud orientatsiooni ja mehaanilist kokkupuudet, nõrgendades keskmist efekti;
Praktilised näited ja tähtsus
- Nobelegaaside vedeldumine ja tahkestumine on peamiselt dispersioonijõudude tulemus — näiteks heeliumi ja argooni aatomite vahel.
- Orgaaniliste ühendite laddumine, sulamispunktid ja keemistemperatuurid sõltuvad suurel määral van der Waalsi interaktsioonidest; suurem molekul = tavaliselt kõrgem keemistemperatuur.
- Valkude ja nukleiinhapete kolmemõõtmeline struktuur ning membraanide kokkupanek on osaliselt tingitud nõrkadest molekulidevahelistest tõmbejõududest.
- Gecko limaskesta imemine ja paljud kleepuvad pinnad töötavad peamiselt arvukate van der Waalsi kontaktide kokkuvõtet arvestades.
- Supramolekulaarne keemia ja molekulaarne eneseorganiseerumine toetuvad sihipärasele van der Waalsi ja dipool-interaktsioonide kasutamisele.
Mõõtmine ja modelleerimine
Van der Waalsi jõude uuritakse katsetega, kasutades näiteks AFM‑i (atomjõu mikroskoop), surface force apparatus’e ja spektroskoopiat. Arvutuskeemias modelleeritakse neid jõude tihti tiitlitega nagu Lennard‑Jonesi potentsiaal, Hamakeri konstant kondenseeritud faasides või keerulisemate rühm‑põhiste jõumudelite abil makromolekulide puhul.
Kokkuvõte
Van der Waalsi jõud on universaalsed, nõrgad, kuid hädavajalikud interaktsioonid, mis mõjutavad aine füüsikalisi omadusi, molekulide kokkupakkumist, bioloogilisi struktuure ja paljusid tehnoloogilisi rakendusi. Kuigi need jõud võivad olla individuaalselt nõrgad võrreldes kovalentsete või ioonsete sidemetega, võib suur hulk nõrku kontakte kokkuvõttes anda märkimisväärse mõju.

