Ensüümid on rakkude valgumolekulid, mis toimivad bioloogiliste katalüsaatoritena. Ensüümid kiirendavad organismis toimuvaid keemilisi reaktsioone, kuid nad ei kasuta end protsessi käigus ära, mistõttu neid saab üha uuesti ja uuesti kasutada.
Peaaegu kõik elusolendite biokeemilised reaktsioonid vajavad ensüüme. Ensüümiga toimuvad keemilised reaktsioonid palju kiiremini kui ilma ensüümita.p39 Teised biokatalüsaatorid on katalüütilised RNA-molekulid, mida nimetatakse ribosüümideks.
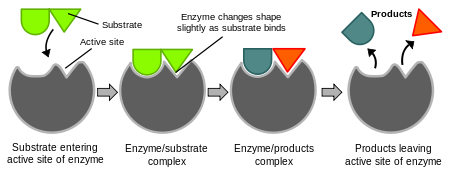
Reaktsiooni alguses olevaid aineid nimetatakse substraatideks. Reaktsiooni lõpus olevad ained on produktid. Ensüümid töötavad substraatidega ja muudavad need toodeteks. Ensüümide uurimist nimetatakse ensümoloogiaks.
Esimene ensüüm leiti 1833. aastal Anselme Payeni poolt.
Struktuur ja toimemehhanism
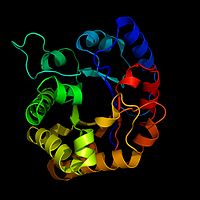
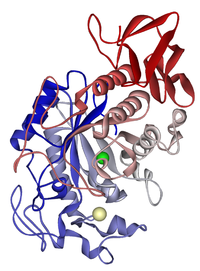
Enamik ensüüme on valgud, millel on keerukas kolmemõõtmeline struktuur. Ensüümidel on aktiivne koht — väike osa valgumolekulist, kuhu substraat seondub. Aktiivses kohas toimub keemiline reaktsioon: ensüüm stabiliseerib üleminekuoleku ja alandab reaktsiooni aktivatsioonienergiat, mis kiirendab reaktsiooni kulgu.
Ensüümide toimemehhanismi kirjeldamiseks kasutatakse sageli mudeleid nagu lukku-ja-võti või kohanduva sobivuse (induced fit) mudelid. Neis seletustes rõhutatakse, et substraat ja ensüüm sobituvad omavahel spetsiifiliselt — ensüüm tunneb ära teatud substraadi või substraatide rühma.
Spetsiifilisus ja tüübid
- Substraat-spetsiifilisus: paljud ensüümid töötavad ainult ühe või mõne väga lähedase substraadiga.
- Reaktsioonispetsiifilisus: mõni ensüüm katalüüsib ainult teatud tüüpi keemilist reaktsiooni (nt hüdrolüüs, oksüdatsioon).
- Peamised ensüümiklassid (IUBMB EC-süsteem): oksüdoreduktaasid, transferaasid, hüdrolaasid, lüaasid, isomeraasid ja ligaasid.
Faktorid, mis mõjutavad ensüümide aktiivsust
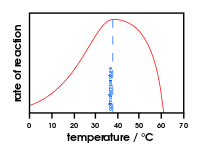
- Temperatuur: igal ensüümil on optimaalse temperatuuri vahemik; liiga kõrge temperatuur võib põhjustada denaturatsiooni (struktuuri hävimist) ja aktiivsuse kaotust.
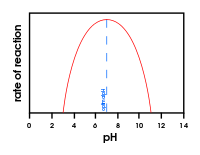
- pH: ensüümid töötavad parimalt teatud pH-l; happeline või aluseline keskkond võib muuta aktiivsete rühmade laengut ja seeläbi aktiivsust.
- Substraadi kontsentratsioon: suurem substraadi sisaldus võib tõsta reaktsiooni kiirust kuni punktini, kus kõik ensüümi molekulid on aktiivses kohas hõivatud (saturatsioon).
- Kofaktorid ja koensüümid: paljud ensüümid vajavad aktiivseks olemiseks täiendavaid mittevalgulisi ühendeid, nt metallioone või orgaanilisi koensüüme (näiteks NAD+, FAD).
- Inhibiitorid: inhibiitorid võivad ensüümi aktiivsust pärssida reversiibselt (konkurentsiline, mittekonkurentsiline) või irreversiibselt (püsiv inaktiveerimine).
Kinetika ja mõõtmine
Ensüümide kineetika kirjeldab, kuidas reaktsiooni kiirus sõltub substraadi ja ensüümi kontsentratsioonist. Levinud mudel on Michaelise–Menten kineetika, kus võtmetähtsusega parameetriteks on Vmax (maksimaalne kiirus) ja Km (Michaelise konstant — substraadi kontsentratsioon, mille juures kiirus on pool Vmax).
Ensüümide aktiivsust mõõdetakse sageli ühikutes (nt üksus = katalüüsitud substraadi hulk ajaühikus) ja laboris kasutatakse spektrofotomeetrilisi, kromatograafilisi või happe-baasi indikaatoreid lähtudes reaktsiooni tüübist.
Bioloogiline ja praktiline tähtsus
- Seedimine: ensüümid nagu amülaas, proteaasid ja lipaasid aitavad toitu lagundada ja imendumiseks ette valmistada.
- Metaboolsed protsessid: ensüümid osalevad ainevahetuses, energia tootmises (nt ATP süntees), DNA replikatsioonis ja parandamises (DNA ja RNA polümeraasid) ning raku signalisatsioonis.
- Meditsiin: ensüümpõhised testid aitavad diagnoosida haigusi (nt maksaensüümid, pankrease ensüümid), ensüümid võivad olla haiguse põhjuseks (ensüümide defitsiidid) või ravimi sihtmärgiks.
- Tööstus ja biotehnoloogia: ensüüme kasutatakse pesupesuvahendites plekieemaldamiseks, toidutööstuses (juustutootmine, leivatööstus), farmaatsias ravimite sünteesiks ja bioloogilises lagundamises.
Ajalugu ja terminoloogia
Esimese ensüümi avastas 1833. aastal Anselme Payen. Hiljem arendati ensüümide mõistmist edasi (sh Emil Fischeri lukku-ja-võti idee ning avastused rakkudest eraldunud ensüümide kohta). Tänapäeval klassifitseeritakse ensüüme rahvusvahelise süsteemi alusel ja neile antakse nimetused, mis peegeldavad katalüüsitavat reaktsiooni (nt laktaas, lipaas, katalaas).
Olulised mõisted lühidalt
- Aktivne koht: ensüümi osa, kus toimub substraadi seondumine ja katalüüs.
- Apoensüüm: valguosa, mis vajab funktsioneerimiseks kaasuvat kofaktorit.
- Holoensüüm: aktiivne ensüüm koos kõigi vajalike kofaktorite/koensüümidega.
- Denaturatsioon: ensüümi struktuuri pöördumatu hävimine soodustingimustes (nt kõrge temperatuur, äärmuslik pH).
Ensüümid on elusorganismide toimimise aluseks — ilma nendeta oleksid biokeemilised protsessid liiga aeglased, et elu säiliks. Nende uurimine ja rakendamine jätkab olulist rolli nii meditsiinis kui tööstuses, pakkudes vahendeid haiguste mõistmiseks, uute ravimite väljatöötamiseks ja keskkonnasõbralike tehnoloogiate loomiseks.