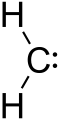Karbeen on molekul, mille keskmes olev süsinikuaatom kannab ainult kahte σ-sidet ja millel on kaks vaba elektroni, mis ei osale sidemete moodustamises. Kuna süsiniku ümber on kokku ainult kuus elektroni, on karbeen väga reaktiivne ja lühiajaline. Üldvalemina kirjutatakse seda sageli kujul R-(C:)-R'.
Struktuur: singlet ja triplet
Karbeen võib eksisteerida kahes põhilises elektronilises olekus: singlet ja triplet. Singlet-karbeeni korral paiknevad kaks mittesiduvat elektroni samas orbitaali (näiteks sp2‑orbitaalis), moodustades paaritu elektronipaar sarnaselt üksikpaarile. Triplet-karbeenis paiknevad need kaks elektroni eri orbitaalides ja neil on sama spinn, mistõttu selline olek on paramagnetiline.
Milline olek on eelistatum, sõltub tugevalt asenditest ja keskkonnast. Lihtsad alküülasendid soodustavad sageli triplet‑olekut (radikaalset iseloomu), samas kui heteroaatomite või halogeenide lähedus ja konjugatsioon võivad singlet‑oleku stabiliseerida. Lisastabiilsus ja ruumiline kaitse mõjutavad samuti oleku eelistust.
Kuidas karbeene sünteesitakse ja kus neid leitakse
Karbeene ei ole tavaliselt isoleeritud kui püsivad ained (välja arvatud erandlikud juhtumid). Levinumad meetodid karbeenide tekeks on:
- diazoühendite termolüütiline või fotolüütiline lagunemine, mille käigus eraldub lämmastik (N2) ja tekib karbeen;
- α‑elimineerumine halogeenitud ühenditest (nt dichloro‑karbeen CCl2 saadakse chloroformist tugeva aluse toimel);
- diaziriinide fotolüüs, mis annab lühiajalisi karbeene;
- metallidega aktsepteeritud dekompositsioon, kus tekib metallo‑karbeen (metalli ja karbeeni vaheline M= C side).
Katalüütilistes reaktsioonides ja sünteetilises keemias on levinud ka metallo‑karbeenide teke diazoühendite lagunemisel metallisoolade või organometallkatalüsaatorite juuresolekul.
Reaktsioonid ja kasutusvaldkonnad
Karbeenidel on lai reaktsioonivalik, sest nad võivad käituda nii elektrofiilidena kui ka nukleofiilidena, sõltuvalt nende elektronilisest iseloomust. Tüüpilised reaktsioonitüübid on:
- Liitumised kaksiksidemetega — karbeenid lisanduvad alkeenidele, tekitades tsüklilisi tooteid (nt cyclopropanatsioon). See on oluline C–C sideme moodustamise viis.
- C–H ja X–H (X = O, N) insertioonid — karbeenid võivad siseneda C–H sidemesse ja tekitada uut C–C sidet; see võimaldab regio‑ ja stereo‑valikuliselt modifitseerida molekule.
- Sügelusreaktsioonid ja ylide‑moodustumine — karbeeni reageerimine fosfiinidega võib anda fosfoonium‑ylide, mida kasutatakse muuhulgas Wittig‑tyypi transformatsioonides.
- Reaktsioonid konjugeeritud süsteemidega ja osalemine ketroopilistes reaktsioonides või muudes pericyklistes protsessides.
Paljud neist reaktsioonidest on sünteetiliselt väga väärtuslikud — näiteks olefiinide metatees, cyclopropanatsioonid ja selektiivsed insertioonid on orgaanilise sünteesi tööriistakomplekti põhielemendid.
Stabiliseerimine ja erinevad tüübid
Enamik väikeseid karbeene on äärmiselt ebastabiilsed ja eksisteerivad vaid väga lühikest aega. Kuid teatud mehhanismid ja struktuurid neid stabiliseerivad, mistõttu on võimalik saada püsivaid või "pikaealisi" karbeene:
- Ruumi- ja elektroniline stabilisatsioon — suured sterilised rühmad takistavad dimeriseerumist ja muudavad karbeeni vähem reaktiivseks; elektroniline delokaliseerimine (näiteks heteroatomite kaudu) stabiliseerib vaba elektronipaari või tühja orbitaali.
- N-heterotsüklilised karbeenid (NHC) — need on tänapäeval tuntud ja isoleeritavad karbeenid, millel on tugevad donoriomadused ja mis toimivad levinud ligandidena organometallkatalüsaatorites ning kui orgaanikatalüsaatorid.
- Metallo‑karbeenid — jagunevad suuresti kaheks tüübiks: Fischer‑ ja Schrock‑karbeenid. Fischer‑karbeenid on üsilektroniliselt pigem elektrofiiilsemad ja seonduvad tihti hiliste üleminekumetallidega, Schrock‑karbeenid on enamasti nukleofiilsemad ja seotud varajaste, kõrges oksüdatsiooniasendis metallidega. Mõlemad tüübid on olulised organometallilises keemias ja katalüüsis.
Praktiline tähtsus ja näited
Mõned karbeenidest ja nendega seonduvatest süsteemidest on eriti tuntud. Näiteks dichloro‑karbeen (CCl2) ja methüleen (:CH2) on klassikalised põkseeksperimentides käsitletavad liigselt reaktiivsed liigid. Samal ajal on NHC‑id erandlikud püsivad karbeenid, mida kasutatakse laialdaselt ligandidena ja kui organokatalüsaatorid.
Metall‑karbeenid on üliolulised katalaasorides: kuulus näide on Grubbs'i katalüsaator, mille tööstusliku ja uurimistöö tähtsuse tõttu tihti seostatakse nimega Robert Grubbs. Grubbs'i tüüpi ruthenium‑karbeenid võimaldavad efektiivset olefiinide metateesi — võimsat meetodit C=C sidemete ümberpaigutamiseks organilises sünteesis.
Uurimismeetodid ja identifitseerimine
Kuna enamik karbeene on väga lühiajalised, uuritakse neid sageli kiiremate spektroskoopiliste meetoditega: EPR/ESR‑spektroskoopia (triplet‑olekute tuvastamiseks), kiiresti segmenteeritav fotolüüs, matrix‑isolation madalatel temperatuuridel ning teised ajaliselt lahutavad tehnikad. Singlet‑karbeene on sageli tuvastatavad NMRi abil (kui piisavalt stabiilsed), tripletid annavad paramagnetilisi signaale.
Kokkuvõttes on karbeenid keemia põnev ja mitmekülgne klass ühendeid: kuigi paljud neist on väga reaktiivsed ja lühiajalised, on olemas myös stabiliseeritud vormid (näiteks NHC‑id ja metallo‑karbeenid), mis on saanud asendamatuks tööriistaks kaasaegses sünteetilises ja organometallilises keemias.