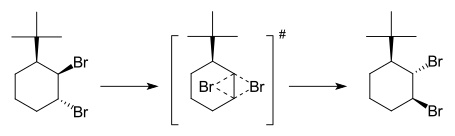
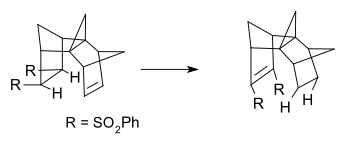
Düotroopne reaktsioon on teatud tüüpi keemiline reaktsioon, kus ühes molekulis toimub kahe rühma samaaegne ümberpaigutumine. Tavaliselt muutub orgaaniline ühend selle tulemusena oma struktuuri—kaks asendajat (migreeruvat rühma) liiguvad samaaegselt ühest kohast teise või vahetavad omavahel positsioone. Seda tüüpi protsessi loetakse peritsükliliseks valentsiisomerisatsiooniks, kui kaks sigma sidet nihkuvad korraga uutesse kohtadesse. Düotroopsed reaktsioonid on orgaanilises keemias olulised nii mehaanika mõistmiseks kui ka keerukate molekulide sünteesisse integreerimiseks. Nimetus on tuletatud kreeka sõnast dyo („kaks“) ning „rearrangement“ viitab aatomite vahelistest sidemetest tingitud ümberkorraldustele. Termi kirjeldas esmakordselt Manfred T. Reetz 1971. aastal.
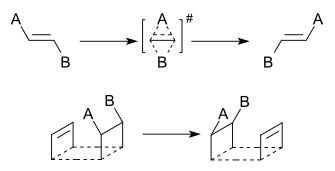
I tüübi mehhanism
I tüübi düotroopse reaktsiooni puhul vahetavad kaks migreeruvat rühma omavahel oma suhtelist positsiooni ahelas. See tähendab, et rühm A liigub kohast X kohale Y samal ajal kui rühm B liigub kohast Y kohale X. Sellised protsessid toimuvad sageli konsertseeritud ehk samaaegse mehhanismina ja läbivad tavaliselt tsüklilise üleminekuoleku (näiteks neljaliikmelise tsükli), kus mõlemad σ-sidemed nihkuvad korraga. Klassikaline näide on vicinaalsete halogeenide ümberpaigutumine (halogeenide „vahetus“) alifaatsetes ahelates.
- Põhiomadused:
- samaaegne (konsertseeritud) kahe sideme migratsioon,
- tsükliline üleminekuolek ja sageli kõrge energia barjäär (seega nõuab sageli kuumutamist),
- võib olla stereosõltuv — konkreetne stereokeemiline tulemus sõltub täpsemast üleminekuoleku geomeetriast.
II tüübi mehhanism
II tüübi düotroopsed reaktsioonid hõlmavad samuti kahe rühma migratsiooni, kuid siinkohal ei toimu rühmade omavahelist positsioonivahetust. Selle asemel liiguvad rühmad uutesse sidumiskohtadesse, nii et lõpptoodangus on rühmade paigutus võrreldes algsega muutunud, kuid nad ei ole üksteisega lihtsalt vahetanud kohad. II tüüpi protsessid võivad toimuda konsertseerdult, kuid mõnel juhul on võimalikud ka samm-sammulised (ionilised või radikaalsed) mehhanismid sõltuvalt rühmade iseloomust ja reaktsiooni tingimustest.
- Erinevused I ja II tüübi vahel:
- I tüüp = otsene positsioonivahetus kahe rühma vahel,
- II tüüp = migratsioon uutesse sidumiskohtadesse ilma otsese vahetuseta.
Mõjurid ja mehhanistlik mitmekesisus
Düotroopseid reaktsioone mõjutavad mitu tegurit:
- Temperatuur — paljud düotroopsed ümberkorraldused vajavad kõrget temperatuuri, et ületada üleminekuoleku energia.
- Substituendid ja elektronilised efektid — elektronegatiivsus, hüpsofilisus/hüperfokaalsus ja konjugeeritus võivad stabiliseerida või destabiliseerida üleminekuolekut.
- Stereokeemia ja lähteühendi geomeetria — rühmade vaheline lähendatus ja sobiv orientatsioon määravad, kas konsertseeritud ülekanne on võimalik.
- Solvendi ja katalüsaatorid — polaarne solvent või vahendav katalüsaator võib soodustada samm-sammulist (ionilist) teed või vähendada aktiveerimisenergiat.
Kuigi sageli kirjeldatakse düotroopseid reaktsioone kui konsertseeritud peritsüklilisi protsesse (tsükliline üleminekuolek, ilma püsivate vaheproduktideta), võivad teatud süsteemid käituda sammsammulise mehhanismi järgi, kui tekib näiteks stabiilsem iooniline või radikaalne vaheprodukt.
Kasutusvaldkonnad ja tähendus
Düotroopsed ümberkorraldused on kasulikud orgaanilises sünteesis, sest need võimaldavad ümberpaigutada rühmi täpselt ja sageli stereospecifiliselt, ilma et oleks vaja katkestada või moodustada uusi funktsionaalseid rühmi. Neid kasutatakse keerukate molekulide konstrueerimisel ja mõnikord ka teadaolevate protektsioonide või rühmade regiosele ümberpaigutamisele. Arusaamine düotroopsetest mehhanismidest aitab selgitada mitmeid looduslikke ja laboritingimustes toimivaid ümberkorraldusi.
Kokkuvõte: düotroopne reaktsioon on kahe asendaja samaaegne ümberpaigutumine molekulis — I tüübis toimub rühmade omavaheline vahetus, II tüübis liiguvad rühmad uutesse kohtadesse ilma otsese vahetuseta. Reaktsioonid võivad olla konsertseeritud peritsüklilised või, teatud tingimustel, samm-sammulised, ning nende mehhanism ja stereokeemia sõltuvad lähteühendi ja tingimuste nüanssidest.