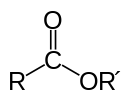
Ester on orgaaniline ühend, mis sisaldab karbonüülrühma (C=O), mille karbonüülisüsinikuga on seotud oksügeen kaudu alküüli- või arüülrühm — üldvalem R–CO–OR'. Rühma võib kirjutada ka kui COOR. Estrid tekivad sageli, kui karboksüülhape reageerib alkoholiga (reageerimisel) happe katalüsaatori juuresolekul; see on üks levinumaid sünteesiviise orgaanilises keemias.
Struktuur ja põhiolemus
Estrite karakterit määrab karbonüüli ja oksügrupi koosmõju. Oksügeen annab karbonüülile osalist elektronidoonust resonantsi kaudu, mistõttu on esteri karbonüül vähem electrophiilne kui näiteks karbonüülrühm hüdroksiidideta karboksüülhapetes või aküülhalogeniidides. See mõjutab estrite reaktiivsust ja nende käitumist nukleofiilsete rünnakute ajal.
Füüsikalised omadused
- Paljud madalama moolmassi estrid on lenduvad ja neil on iseloomulikud, sageli meeldivad lõhnad — seda kasutatakse maitse- ja lõhnaainete tootmisel.
- Estrite lahustuvus vees sõltub ahela pikkusest: lühemad estrid (nt metüül- ja etüülestrid) on vees mõõdukalt lahustuvad, pikemad on vees praktiliselt lahustumatud.
- Keemistemperatuurid ja polaarsus jäävad tavaliselt alkoholide ja ketoonide vahele; esteri süsinik-oksiidi sidemete vibratsioonid annavad spetsiifilised signaalid spektroskoopias.
- Estrid võivad olla hüdrolüüsi suhtes nii happelise kui aluseliselt katalüüsitud; aluselise hüdrolüüsi (saponifikatsioon) on sageli pöördumatu ja annab seebi/soola ning alkoholi.
Süntees
Peamised sünteesimeetodid:
- Fischeri esterifikatsioon — karboksüülhappe ja alkoholi reageerimine happelise katalüsaatori (nt H2SO4) juuresolekul, tasakaalureaktsioon, vee eemaldamine suurendab saaki.
- Acüülhalogeniidide või anhhüdriidide kasutamine — reageerimine alkoholiga annab esteri tavaliselt kergemini ja suurema saagiga kui otse hapoest lähtuv esteriifikatsioon.
- Transesterifikatsioon — ühe esteri alkohoolsest osast teise alkoholi vahetus; oluline polümeeritööstuses ja biodiisli tootmises.
- Enzymaatiline (biokatalüütiline) esterifikatsioon — lipaaside kasutamine sobib õrnemate tingimuste ja regiosele/enantiosele valikulisuse saavutamiseks.
Olulised reaktsioonid
- Nukleofiilne aküülasend (nukleofiilne liitumine ja OR'-rühma väljatõrjumine) — üldine mehhanism estrite keemias.
- Hüdrolüüs — happelise või aluselise katalüüsiga, annab tagasi karboksüülhappe ja alkoholi; aluselise hüdrolüüsi korral (saponifikatsioon) tekib karboksülaadi sool.
- Reduktsioon — tugevate redutsentidega (nt LiAlH4) reduktsiooni produkt on primaarne alkohol. Poolpehmemad redutseerijad nagu DIBAL-H võimaldavad esteri konverteerimist aldehüüdiks kontrollitud tingimustel.
- Konversioon ketooniks — võimalik nt organokupraatide (Gilman reagendid) või muude spetsiifiliste reagentside abil, kuid nõuab eritingimusi.
Kasutusalad
Estrid on laialt levinud nii looduses kui tehnoloogias:
- Toidu- ja lõhnaained: paljud puuvilja- ja lillelõhnad on estrid; neid kasutatakse parfüümide ja maitseainete valmistamisel.
- Solvendid: nt etüülatsetaat ja metüülatsetaat on levinud orgaanilised solventid.
- Füüsilised lipiidid: rasvad ja õlid on peamiselt glütseriini triesterid ehk triglütseriidid.
- Polüestrid: polüestreid kasutatakse kiududes, plastides ja tehnilistes rakendustes (näiteks PET). Samuti on olemas biolagunevad ester-polümeerid (nt polülaktiid).
- Biodiisel: transesterifikatsioonitransformatsioon taimsetest/loomsetest õlidest alküül-estriteks (metüül- või etüülestriteks).
- Plastiseerijad ja katteained: teatud esterid muudavad polümeere paindlikumaks või annavad spetsiifilisi omadusi.
Analüüs ja identifitseerimine
On mitmeid meetodeid, kuidas tuvastada esterrühma molekulis:
- Infrapunaspektroskoopia (IR) annab teravad signaalid: esteri karbonüüli tõmme esineb tavaliselt ~1735–1750 cm−1 (alifaatsetel estritel); konjugatsioon ja rõhuasetus võivad seda nihutada. Samuti esinevad tugevad C–O venimised 1050–1300 cm−1.
- 1H ja 13C NMR-spektroskoopia — Süsiniku NMR näitab esteri karbonüüli signaali umbes 160–185 ppm (tüüpiliselt ~165–175 ppm esterde puhul). 1H NMR-is ilmuvad O–CH2 või O–CH3 signaalid tavaliselt ~3,5–4,5 ppm ulatuses (sõltuvalt asendustest).
- Gaasspektromeetria (GC–MS) — hea madalmolekulaarsete lenduvate estrite identifitseerimiseks ja kvantifitseerimiseks, eriti lõhnaainete analüüsis.
- HPLC, titrimine ja keemilised reaktsioonid — hüdrolüüsi abil saab tuvastada ja kvantifitseerida estereid; saponifikatsioon kärpib esterrühma ja võimaldab määrata rasvu/õlisid.
Ohutus ja keskkonnamõju
Mõned estrid on tuleohtlikud, võivad ärritada nahka või limaskesti ning sissehingamisel mõnel juhul olla toksilised. Paljudes tööstuslikes protsessides tuleb vältida otsest kokkupuudet ning tagada piisav ventilatsioon ja kaitsevahendid. Samuti on olulised keskkonnamõjud: laialdaselt kasutatud plastiseerivad ja sünteetilised ester-polümeerid võivad keskkonda kuigi aeglaselt mõjutada, samas kui biolagunevad ester-polümeerid arenevad vastu kasvava huvi tõttu.
Kokkuvõttes on estrid keemiliselt mitmekülgsed ühendid, millel on mitmeid võimalikke sünteese ja rakendusi — alates maitse- ja lõhnaainetest kuni plastitööstuse ja biokütusteni. Nende iseloomulikud spektraalsed tunnused ja reaktsioonskeemid teevad neist olulise rühma nii analüütilises kui sünteetilises orgaanilises keemias.