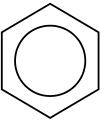
Aromaatsed süsivesinikud ehk areenid on süsivesinike rõngaste ühendid. Nendes ühendites esinevad rõngas vaheldumisi kaksik‑ ja ühekordsed sidemed süsinikuaatomite vahel, moodustades stabiilse delokaliseeritud elektronpilve. Paljudel aromaatsel ühendel on terav või magus lõhn — sellest tulenebgi nimetus "aromaatne". Kuuest süsinikuaatomist koosnevat rõngast aromaatsetes ühendites nimetatakse benseeniringiks, mis on lihtsaim ja klassikaline näide — benseeni järgi nimetatuna. Aromaatsed süsivesinikud jagunevad üldiselt monotsüklilisteks (MAH) ja polütsüklilisteks (PAH).
Mõned mitte‑benseenipõhised ühendid, mida nimetatakse heteroareenideks ja mis järgivad Hückeli reeglit, on samuti aromaatsed. Nendes aatomiraamistikus on vähemalt üks süsiniku aatom asendatud teiste elementidega, näiteks hapniku, lämmastiku või väävli aatomiga — tuntud näited on furaan, püridiin ja tiofeen.
Struktuur ja aromaatsuse põhialused
Aromaatsus tuleneb elektronide delokaliseerumisest rõnga kohal — pi‑elektronid jagunevad üle kogu tsükli, mis annab ühendile tavaliselt suurema stabiilsuse kui analoogne avatud ahela ühend. Selle elektronide arv ja konjugatsioon peab vastama Hückeli reeglile (4n + 2 π‑elektroni), et rõngas oleks aromaatne. Aromaatse rõnga geomeetria on tavaliselt planaarne või peaaegu planaarne.
Füüsikalised omadused
- Enamik areene on hüdrofoobsed, lahustuvad hästi orgaanilistes lahustites, kuid mitte vees.
- Paljudel on iseloomulik, tihti terav või magus lõhn.
- Polütsüklilised aromaatsed süsivesinikud (PAH) kipuvad olema tahkestaolised ja madalama lahustuvusega vees kui lihtsamad monotsüklilised areenid.
Keemilised omadused ja reaktsioonid
Aromaatilised rõngad osalevad peamiselt elektrofiilses asendamises (nt nitreerimine, sulfoneerimine, halogeenimine), kus säilib rõnga aromaatsus. Teised võimalikud reaktsioonid hõlmavad erütseeritust (hydrogenatsiooni) — täielikuks küllastumiseks peab hapnik või katalüsaator murdma aromaatse delokaliseerimise — ning erinevaid lisareaktsioone, oksüdatsiooniid ja radikaalprotsesse.
Tüübid ja näited
- Monotsüklilised areenid — benseen, toluen, ksüleenid jt (MAH).
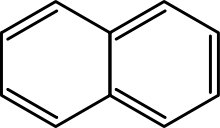
- Polütsüklilised areenid — naftaleen, antratseen, fenantrseen ja mitmed suuremad PAH‑ühendid (näiteks benzo[a]püreeni); need koosnevad omavahel liitunud mitu aromaatset rõngast.
- Heteroareenid — püridiin, furaan, tiofeen jpt, kus on vähemalt üks mitte‑süsiniku aatom.
Tervise‑ ja keskkonnamõjud
Paljud areenid, eriti mõned PAH‑ühendid, on tuntud toksiliste ja kantserogeensete omaduste poolest (näiteks benzo[a]püreeni puhul). PAH‑e tekib ebatäiusliku põlemise tulemusel — kütuste, puidu, sigarettide, tööstusprotsesside ja liiklusheitmete kaudu. Nad on keskkonnas püsivad, võivad akumuleeruda mullas ja setetes ning sattuda toiduahelasse.
Kasutusvaldkonnad ja ohutus
Aromaatseid ühendeid kasutatakse laialdaselt keemiatööstuses: lahustitena (nt benseen, toluen), keemilisteks lähteaineteks plastide, värvainete, pestitsiidide ja ravimite tootmisel. Samas nõuavad paljud neist tugevamat kontrolli ja ohutusmeetmeid, sest paljud monomereid või kõrvalprodukte peetakse ohtlikeks.
Ohutussoovitused labori‑ ja tööstusolukorras:
- Väldi sissehingamist ja nahakontakti — kasuta sobivaid respiraatoreid, kinnast ja kaitseprille.
- Kasutada hästi ventileeritud ruume või kappe.
- Jälgida tööstuse ja keskkonnaalaseid juhiseid PAH‑ide emissiooni ja eemaldamise kohta.
Analüüs ja regulatsioon
PAH‑e ja teisi areene mõõdetakse gaasikromatograafia, massspektromeetria ja teiste analüütiliste meetoditega. Paljudel riikidel on norme ja piirväärtusi õhus, vees ja toidus sisalduvate PAH‑ide osas, et vähendada inimeste kokkupuute riske.
Kokkuvõtteks: aromaatsed süsivesinikud on keemiliselt eripärased ja laialt kasutatavad ühendid, mille unikaalne delokaliseeritud elektronstruktuur annab neile stabiilsuse ja iseloomuliku keemia. Samas vajavad mõned neist, eriti polütsüklilised aromaatsed süsivesinikud, tähelepanu ohutuse ja keskkonnakaitse seisukohalt.