Orgaanilises keemias toimub liitumisreaktsioon, kui kaks molekuli ühinevad, et moodustada suurem molekul. See saab toimuda ainult siis, kui ühel molekulist on juba kaksik- või kolmikside. Need võivad olla süsinik-süsinik sidemed või isegi süsinik-hapnik, süsinik-tüüner ja muud. Üht kahest molekulist nimetatakse nukleofiiliks ja see on see, mis annab teisele molekulile elektronid, et luua uus side. Teist molekuli nimetatakse elektrofiiliks ja see on see, mis saab elektronid.
Liitumisreaktsioon on eliminatsioonireaktsiooni vastand. Tavalised näited liitumisreaktsioonidest on vee liitumine üle kaksiksidemete ja nukleofiilne rünnak karbonüülile.
Põhiliigid
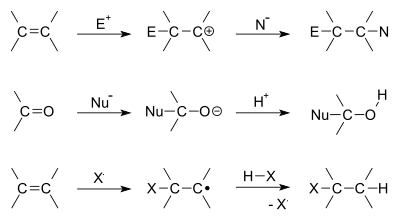
- Elektrofiilne liitumine – tüüpiline alkeenide reaktsioon: elektrofiil ründab kaksiksidet ja tekib vaheühend (nt karbokation), millele järgneb nukleofiilne liitumine.
- Nukleofiilne liitumine – tavaline karbonüülühendite (aldehüüdid, ketoonid) puhul: nukleofiil ründab süsinikku ja moodustub tetraeedriline vaheühend.
- Radikaalne liitumine – toimub radikaalide kaudu (initsiaatorid, valgus või temperatuur), näiteks peroksiidide abil algatatud liitumised.
- Tsükloaddition – kahe või enama multiple sideme üheaegne liitumine, nt Diels–Alder reaktsioon (konjugeeritud dioleen + alkeen → tsükliline produkt).
- Liitumispolümerisatsioon – monomeeride liitumine ühesuunaliselt, malliks näiteks etüleeni polümerisatsioon kokku polüetüleeniks.
Mehhanism ja vaheühendid
Liitumisreaktsioonide mehhanism võib olla samm-sammuline või konsertne (sünkroonne). Levinumad vaheühendid ja mehhanisme mõjutavad osakesed on:
- Karbokatsioonid – tekivad elektrofiilses liitumises olulisel kohal; nende stabiilsus määrab regio- ja stereokeemiat.
- Radikaalid – osalevad radikaalsetes liitumistes, nende teket ja lagunemist kontrollivad initsiaatorid ja tingimused.
- Karbanioonid ja oksaanioonid – võivad tekkida nukleofiilses liitumises, eriti tugevate nukleofiilide korral.
- Tetraeedrilised vaheühendid – karbonüülide nukleofiilsel rünnakul tekkinud vaheolek, misjärel toimub protoneerimine või muud ümberkorraldused.
Orbitaalide vaatenurgast on oluline HOMO–LUMO vastastikmõju: nucleofiili HOMO ja elektrofiili LUMO ühilduvus soodustab liitumist. Katalüsaatorid (happed, metallid) ja tingimused (temperatuur, lahusti) mõjutavad reaktsiooni kulgu ja valikulist tulemust.
Regio- ja stereokeemia
- Markovnikovi reegel kirjeldab, kuhu lisandub H‑atom alkeni liitumisel (H läheb enam H‑substitueeritud süsiniku poolsemale positsioonile vähemasti): sellest tuleneb regioselektiivsus mitmetes elektrofiilsetes liitumistes.
- Anti‑Markovnikovi lisandumine võib toimuda radikaalsete mehhanismide või peroksiidide juuresolekul (nt HBr + peroksiid).
- Syn vs anti lisandumine – stereokeemiline tulemus sõltub mehhanismist: näiteks halogeenide lisandumine kaksiksidemele möödub sageli anti‑moodusel (vastaspoolt), vesinikud metallkatalüütilisel hüdreerimisel lisanduvad syn‑moodusel (samalt poolt).
Näited ja rakendused
- Elektrofiilne hüdraatimine: alkeen + H2O (happes) → alkohol (nt etüleen → etanool happe katalüüsil).
- Hydrohalogenation: alkeen + HBr → bromoalkaan (Markovnikovi regioselektiivsus; peroksiidide olemasolul võib saada anti‑Markovnikovi toodet).
- Halogeenimine: Br2 või Cl2 lisandumine kaksiksidemele → 1,2‑dihalogenide (tavaliselt anti‑lisandumine, bromonium‑iooni vaheühend).
- Hüdreerimine (hydrogenation): alkeen + H2 (metallikatalüsaator, nt Pt, Pd) → aluskan; oluline tööstuslik protsess (nt küllastamine, rafineerimine).
- Epoksüdeerimine ja následne avamine: alkeen → epoksiid → nukleofiilne avamine annab regio- ja stereokeemiliselt määratletud alkoholid või teised funktsionaalsed ühendid.
- Diels–Alder: konjugeeritud dioleen + dienofiil → tsükliline toode; väga tähtis sünteesimeetod orgaanilises sünteesis ja ravimikeemias.
- Nukleofiilne lisandumine karbonüülidele: Grignard‑reaktsioonid (R–MgX ründab aldehüüdi/ketooni → pärast hüdrolüüsi alkohol), hüdride lisandumine (NaBH4, LiAlH4) annab alkoholid.
- Polümerisatsioon: etüleen → polüetüleen, propüleen → polüpropüleen; lisa‑polümerisatsioon (addition polymerization) on plastitööstuse põhialus.
Tingimused ja katalüsaatorid
Reaktsiooni kiirus ja valikuline tulemus sõltuvad lahustist, temperatuurist, ainetihedusest ja katalüsaatorist. Happed soodustavad elektrofiilseid liitumisi; metallid (nt Ni, Pd) katalüüsivad hüdreerimist; radikaalsetes liitumistes kasutatakse initsiaatoreid (peroksiidid, UV‑valgus).
Tähtsus
Liitumisreaktsioonid on orgaanilise keemia keskne osa: nende abil saab üles ehitada uusi sidemeid ja keerukaid molekule, valmistada ravimeid, põllumajanduskemikaale, polümeere ning paljusid muud liiki materjale. Mõistmine, kuidas ja miks erinevad mehhanismid toimivad, võimaldab keemikutel valikuliselt sünteesida soovitud struktuure.
Kokkuvõte
Liitumisreaktsioonid hõlmavad molekulide liitumist uue sideme tekitamiseks ja võivad toimuda mitme mehhanismi kaudu (elektrofiilne, nukleofiilne, radikaalne, tsükloaddition). Reaktsiooni regio- ja stereokeemia sõltuvad vaheühenditest (karbokationid, radikaalid, tetraeedrilised anioonid), katalüsaatoritest ja tingimustest. Nende reaktsioonide mõistmine on vajalik orgaanilise sünteesi ja tööstuslike protsesside planeerimiseks.