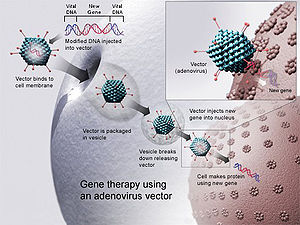
Geeniteraapia tähendab toimiva geeni sisestamist inimesele, kellel on kahjustatud geen. Euroopa Komisjon on selle meetodi heaks kiitnud ühe konkreetse ravi puhul. Ravim Glybera kasutab viirust, et nakatada lihasrakud toimiva geenikoopiaga. Euroopa Komisjon on andnud Glyberale müügiloa, mis tähendab, et seda võib müüa kogu ELis.
Ühel inimesel miljonist on rasvade lagundamiseks vajaliku lipaasigeeni kahjustatud koopia. Rasv koguneb nende veres; see põhjustab valu ja kõhunäärmepõletikku (pankreatiit). See on eluohtlik. Siiani on ainus viis selle haiguse ohjamiseks väga madala rasvasisaldusega toitumine.
Sellisel viisil kasutatuna on viirus vektor. See tähendab, et see on kandja; geen on sisestatud viiruse genoomi ja viirus kleebib selle inimese rakkudesse. Seda tehnikat nimetatakse transfektsiooniks. See tehnika erineb geenide väljaütlemise tehnikast, mille puhul ei kasutata viirusvektorit.
Glybera — konkreetse haiguse raviks loodud geeniteraapia
Glybera (alipogene tiparvovec) oli maailma üks esimesi heaks kiidetud geeniravimeid, suunatud harvaesineva lipoproteiini lipaasi puudulikkuse (LPL-defitsiit) raviks. Ravimi toimepõhimõte on sisestada toimiv lipaasigeen lihasrakkudesse, et taastada või suurendada lipaasi tootmist ja vähendada veres olevate rasvade taset. Seda tehti tavaliselt intramuskulaarsete süstidega valitud lihasekulgudesse.
Milline viirusvektor kasutati ja miks
Adeno-assotsieerunud viirus (AAV) – Glybera puhul kasutati AAV1 serotüüpi. AAVid on populaarne valik, sest neil on mitmeid eeliseid: nad nakatavad rakkusid efektiivselt, tekitavad tavaliselt vähem patoloogilist immuunvastust kui paljud teised viirused ning nende risk juhuslikuks genoomi sissetulekuks (insertional mutagenesis) on madalam kui mõnel teisel klassikalisel vektoril. Samas ei ole AAVid täielikult riskivabad — olemas on immuunvastuse ja eelnevate antikehadega seotud piirangud, mis võivad vähendada ravi efektiivsust.
Ohud, piirangud ja regulatsioon
- Ohud: võimalikud kõrvaltoimed hõlmavad lokaalset põletikku süstekohal, süsteemset immuunvastust, ning harvemini tõsisemaid reaktsioone. Geneetilise materjali püsiv integreerumine on AAVide puhul harvem kui retroviiruste puhul, kuid täielikku riskivabadust see ei taga.
- Püsivus: sõltuvalt vektorist ja koest võib geeni väljund olla ajutine või püsiv — lihasrakus võib ekspressioon kesta aastaid, kuid mõnel juhul väheneb see aja jooksul.
- Piirangud: kõrged kulud ja spetsiifilised patsiadikriteeriumid vähendavad ravi laialdast kasutust.
- Regulatsioon: geeniravi heakskiit ja järelvalve on ranged. Euroopas andis Euroopa Komisjon turustusloa Glyberale, kuid arvestatakse pikajalist jälgimist ja riskide hindamist.
Tulemused ja edasised arengud
Glybera näitas, et somaatiline geeniteraapia võib ravida pärilikke ainevahetushaigusi, kuid praktilised ja majanduslikud takistused olid olulised: ravimi hind oli väga kõrge ja patsientide arv väike, mistõttu tootja hiljem turult taastus. See kogemus on siiski avanud teed edasistele geeniravidele ja arendanud edasi vektorite ning tarneviiside teadust.
Tulevik
Tulevikus oodatakse parandusi viirusvektorites (parem sihtimine, väiksem immuunvastus), samuti mitteviiruslikes tarnekanalites (nt lipiidnanosoomid) ja täpsemates geneetilises redigeerimises (nt CRISPR/Cas-põhised lähenemised). Oluline on jätkuv ohutus- ja tõhususkontroll, eetilised arutelud (eriti eraldades somaatilise ja germline-ravi) ning ligipääsetavuse küsimused, et need uuendused jõuaksid laiemalt patsientideni.