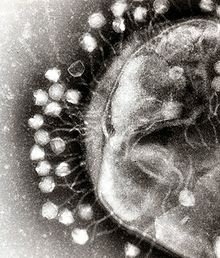
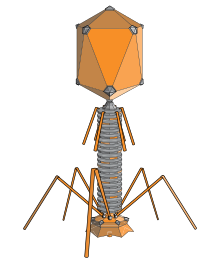
Bakteriofaag on viirus, mis nakatab baktereid. Terminit lühendatakse tavaliselt faagiks.
Bakteriofaagid on ühed kõige levinumad ja mitmekesisemad olendid biosfääris. Sarnaselt eukarüootide (taimed, loomad ja seened) viirustega on faagide struktuurid ja funktsioonid väga erinevad.
Faagid koosnevad tavaliselt väliskestast, mille sees on geneetiline materjal. Geneetiline materjal võib olla üheahelaline (ssRNA või ssDNA) või kaheahelaline (dsRNA või dsDNA). See võib olla 5 kuni 500 kilobaasipaari pikk ja kas ringikujulise või lineaarse paigutusega. Bakteriofaagide suurus on tavaliselt 20 kuni 200 nanomeetrit.
Faagide genoomid võivad kodeerida nii vähe kui neli geeni, aga ka sadu geene. Faagid süstivad oma genoomi bakterisse ja paljunevad bakteri sees.
Faagid on kõikjal, kus on bakterid, näiteks pinnases või loomade soolestikus. Nad on väga levinud merevees: pinnal asuvates mikroobimattides on leitud kuni 9×108 viirust milliliitri kohta ning kuni 70% merebakteritest võib olla faagidega nakatunud.
Neid on kasutatud juba üle 90 aasta antibiootikumide alternatiivina endises Nõukogude Liidus ja Kesk-Euroopas, samuti Prantsusmaal. Kuid alles siis, kui Helmut Ruska 1939. aastal täheldas esimest faagi elektronmikroskoobi all, tehti kindlaks selle tõeline olemus.
Need on võimalik ravi paljude bakterite antibiootikumiresistentsete tüvede vastu. Teisest küljest raskendavad mõned faagid kopsupõletiku ja tsüstilise fibroosi puhul esinevaid biokilesid. Nad kaitsevad baktereid ravimite eest ja pikendavad seega infektsiooni.
Faagide ülesehitus
Bakteriofaagidel on tavaliselt mitmeosaline ehitus: mütsikujuline (kapsiid) proteiinkest, mis sisaldab geneetilist materjali, ning paljudel faagidel ka sabaehitis, mis aitab kinnituda bakteriraku pinnale ja süstida genoomi. Saba võib olla keerukas koos tail fibers-e ja alusplaadiga, mis tunnevad ära bakterispetsiifilised pinnamolekulid.
Geneetilise materjali tüüp (ssDNA, dsDNA, ssRNA, dsRNA), genoomi suurus ja geenide arv võivad faagitüübiti väga erineda – mõned faagid kannavad vaid paar geeni, teised sadu. Faagide morfoloogia ja genoomi ülesehitus määravad suuresti ka nende nakatumismehhanismi ja vaenluse ulatuse.
Elutsükkel: lüütiline ja lüsogeenne
Faagide kaks peamist elutsüklit on lüütiline ja lüsogeenne (temperaatne). Lüütalistes tsüklites paljunevad faagid kiiresti, lüüsivad ehk lõhuvad peremeesbakteri ja vabastavad hulga uusi faage. Lüsogeensete ehk temperaatsete faagide genoom aga integreerub bakteri kromosoomi või püsib ringleva episoomina, olles mitmeid jagunemisi latentsena kuni tingimused soodustavad lüütilisse faasi sisenemist.
Lisaks esineb ka pseudolüsoogia ning faagide vahel on keerulisi regulatsioone (repressioon, indutseerumine). Faagid võivad viia kaasa ka transduktsiooni — teiste bakterite geenide ülekandmist — mis mõjutab mikroobide evolutsiooni.
Levik ja ökoloogiline roll
Faagid on ülipopulaarsed kõikides bakteririkkaes keskkondades: ookeanid, järved, pinnas, taimede ja loomade mikrobioomid. Nad mõjutavad bakteripopulatsioonide tihedust, geneetilist mitmekesisust ja biogeokeemilisi tsükleid (nt süsi ja lämmastik). Lämmatades teatud baktereid, suudavad faagid mõjutada mikroobikommuuni koostist ja toiduahelaid.
Lisaks toodavad mõned faagid ensüüme (nt polüsahhariidide depolümeraasid), mis aitavad neil tungida biofilmidesse — see omadus tekitab nii ravi- kui ka probleemivõimalusi.
Faagiravi (faagiterapia)
Faagiravi tähendab bakteriofaagide kasutamist bakteriaalsete infektsioonide raviks. Ajalooliselt on faage kasutatud alates 20. sajandi algusest: Felix d'Hérelle ja teised kasutasid faage kliiniliselt juba enne antibiootikumide avastamist. Nõukogude Liidus ja Ida-Euroopas säilis faagiterapeutiline praktika laialdasemalt, samas kui lääneriikides võeti see uuesti käsile alles hiljuti, kasvava antibiootikumiresistentsuse tõttu.
Faagide eelised:
- Väga suur täpsus: faagid nakatavad sageli ainult konkreetseid bakteriliike või -tüvesid;
- Võime lüütiliselt hävitada baktereid, sealhulgas biofilmides;
- Vähem kõrvaltoimeid eukarüootsele peremehele võrreldes paljude laia spektriga antibiootikumidega;
- Võimalus kombineerida faagid antibiootikumidega või kasutada faagikokteile ning kohandada teraapiat vastavalt infektsioonile.
Rakendusviisid võivad hõlmata paikset (haavade, nahainfektsioonide), suukaudset, inhaleeritavat (kopsuinfektsioonid) või intravenoosset manustamist, sõltuvalt infektsiooni asukohast ja faagi omadustest. Tänapäeval käib intensiivne uurimistöö kliiniliste katsete, tootmise standardite (GMP) ja regulatiivsete raamistikute arendamiseks.
Ohud, piirangud ja julgeolekuküsimused
Kuigi faagiravi on paljutõotav, on mitmeid piiranguid ja riske:
- Spetsiifilisus tähendab, et ühe faagi efekt võib olla kitsas — sageli on vaja “faagikokteile” või personaalset lähenemist;
- Bakterid võivad arendada resistentsust faagide vastu (näiteks muutuvad retseptorid), kuigi see võib mõnikord muuta neid antibiootikumitundlikumaks;
- Temperaatsete faagide kasutamine on riskantne, sest nad võivad kanduda ja aktiveeruda lüsogeenselt ning potentsiaalselt edasi kanda ohtlikke geene (nt toksiinigeene) — seetõttu eelistatakse sageli lüütilisi faage;
- Faagide kiire bakteri lüüsi tõttu võib vabaneda endotoksiine (G- bakterite puhul), mis võib ärritada immuunsüsteemi;
- Regulatoorne raamistik ja kvaliteedikontroll on endiselt väljakutse — faagitervised peavad olema ohutud, puhastatud ja stabiilsed.
Faagid ja biofilmid
Biofilmides võivad mõned faagid aidata baktereid hävitada, kuna teatud faagid toodavad depolümeraase, mis lagundavad biofilmi maatriksi. Samas on kirjeldatud juhtumeid, kus faagid selekteerivad biofilmi-kaitsvamaid bakteriliike või muidu muudavad mikroobide käitumist, mis raskendab ravi — seetõttu on konkreetse juhtumi uuring vajalik.
Teadusuuringud ja tulevik
Uuringud faagide alal hõlmavad faagide genoomika, immunoloogilist vastust, kombineerimist ravimitega ja faagide geneetilist modifitseerimist sihitud toime parandamiseks. Faagide kasutamine biotehnoloogias (nt faagdisplay, sihtmärkide tuvastus) on samuti laialt levinud.
Tulevikus võib faagiravi muutuda standardseks abimeetodiks teatud ravikindlate infektsioonide korral, kuid selle jaoks on vaja rohkem kliinilisi uuringuid, rangemat regulatsiooni ja tööstuslikku tootmist vastavalt kvaliteedistandarditele.
Kokkuvõte
Bakteriofaagid on ühed kõige arvukamad ja bioloogiliselt olulised viirused Maal, omavad tähtsat rolli mikroobide reguleerimisel ja pakuvad perspektiive alternatiivina või täiendina antibiootikumidele. Nende potentsiaali tuleb kasutada hoolikalt: sobivate faagiliikide valik, ohutuse testid ja regulatiivne kontroll on edu eeltingimused faagiravi laiemaks rakendamiseks.