Keemiline kineetika, mida nimetatakse ka reaktsioonikineetikaks, uurib, kui kiiresti toimuvad keemilised reaktsioonid. See hõlmab ka selle uurimist, kuidas erinevad tingimused, näiteks temperatuur, rõhk või kasutatav lahusti, mõjutavad reaktsiooni kiirust. Keemilist kineetikat saab kasutada ka reaktsioonimehhanismide ja üleminekuolekute väljaselgitamiseks. Lisaks kirjeldab kineetika, kuidas muutuva aja jooksul muutuvad reagendi ja produendi kontsentratsioonid ning kuidas neid muutusi kasutatakse praktikas reaktsiooni juhtimiseks ja optimeerimiseks.
Mõisted ja algpõhimõtted
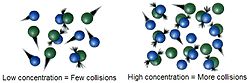
Keemilise kineetika põhiideed nimetatakse kokkupõrketeooriaks. See väidab, et reaktsiooni toimumiseks peavad molekulid omavahel kokku põrkuma. Reaktsiooni kiiruse suurendamise viisid peavad seega suurendama kokkupõrgete arvu. Seda saab teha mitmel viisil: tõsta temperatuurit, suurendada kontsentratsiooni, vähendada ruumala või lisada katalüsaatorit, mis muudab kokkupõrgete efektiivsemaks.
Kiiruse seadused ja kiiruskonstandid
Katsete abil on võimalik arvutada reaktsioonikiirusi, millest saab kiiruse seadused ja kiiruskonstandid. Kiiruse seadus on matemaatiline avaldis, mille abil saab arvutada reaktsiooni kiirust, arvestades reaktiivide kontsentratsiooni. Üldkujul on kiiruse seadus
v = k [A]^m [B]^n …, kus v on reaktiivsuse kiirus, k on kiiruskonstant ja m, n on reaktsiooni järud vastavate reagentide suhtes. Need järud ei pruugi vastata stekiomeetriale ning leitakse eksperimentaalselt.
Olulised punktid kiiruskonstandi ja kiiruse seaduste kohta:
- Kiiruskonstandi k ühikud sõltuvad reaktsiooni järust (nt esimese järgu puhul s⁻¹, teise järu puhul mol⁻¹ L s⁻¹).
- Nulljärk: kiirust ei mõjuta kontsentratsioon (v = k).
- Esimene järk: kiirus on proportsionaalne ühe reagendi kontsentratsiooniga (v = k[A]). Seda kirjeldab integreeritud seadus ln[A] = -kt + ln[A]₀ ja poolväärtusaeg t₁/₂ = ln2 / k.
- Teine järk: võimalikud kujud v = k[A]² või v = k[A][B], mille integreeritud kujud on erinevad.
Temperatuuri mõju ja Arrheniuse seadus
Temperatuur mõjutab tugevalt reaktsioonikiirust. Selle kirjeldamiseks kasutatakse tavaliselt Arrheniuse võrrandit:
k = A · e-Ea/RT, kus A on sagedustegur (sookehi), Ea aktivatsioonienergia, R universaalne gaasikonstant ja T absoluuttemperatuur. Graafik ln k vs 1/T annab sirgjoone, mille kaldenurk võimaldab määrata Ea.
Reaktsioonimehhanismid ja üleminekuriik
Kiiruse seadus annab vihjeid mehhanismi kohta. Paljud reaktsioonid ei toimu üheainsa sammuna, vaid koosnevad elementaarprotsessidest. Iga elementaarne samm on lihtne ja selle korral saab kiiruse avaldada otseselt reagentide kontsentratsioonide kaudu. Mehaanikat uuritakse, otsides:
- elementaarastmeid ja võimalikku piiravat sammu (rate-determining step),
- vaheühendeid või radikaale, mis võivad tekkida ja kuluda reaktsiooni käigus,
- üleminekuoleku omadusi ja kuidas katalüsaatorid vähendavad aktivatsioonienergiat, muutes alternatiivse ja madalama energiaga reaktsioonitee kättesaadavaks.
Mõisted: psuedo-esimene järk ja ketireaktsioonid
Mõnikord hoitakse ühe reaktiivi kontsentratsioon märkimisväärselt suure (nt vastupool), nii et selle muutust ei arvata — sellist olukorda nimetatakse psuedo-esimese järgu tingimuseks ja kiirus näib olevat esimese järjest. Samuti on olulised ketireaktsioonid, mis hõlmavad radikaalseid samme ja võivad sõltuvalt tingimustest käituda kompleksselt (näiteks plahvatuseline või enesekestuv käigus).
Meetodid kiiruse mõõtmiseks ja andmete analüüs
Levinud meetodid reaktsioonikiiruste määramiseks:
- Algkiiruse meetod (initial rates) — mõõdetakse kiirus väikeste ajavahemike jooksul alguses;
- Integreeritud kiiruse seaduste sobitamine — sobitatakse andmed esimese või teise järu lahendustele;
- Spektrofotomeetria ja stopp-voog (stopped-flow) — kiirete reaktsioonide jälgimiseks;
- Gaasikromatograafia või HPLC — kontsentratsioonide jälgimiseks aeg-põhiselt.
Andmete analüüsuks kasutatakse sageli lineaarset teisendust (nt ln[A] vs t esimesel järgul) või mittelineaarset sobitamist, samuti Arrheniuse diagrammi temp sõltuvuse analüüsiks.
Katalüüs ja pinnareaktsioonid
Katalüsaatorid kiirendavad reaktsioone, langetades aktivatsioonienergiat või pakkudes alternatiivse mehhanismi. Katalüüs võib olla homogeenne (katalüsaator on samas faasis kui reagendid) või heterogeenne (nt tahke katalüsaator pindamisel toimub adsorptsioon ja desorptsioon). Pinnal toimuvad sammud (adsorptsioon → reaktsioon → desorptsioon) on tüüpilised näiteks katalüütilisele otooksüdatsioonile ja tööstuslikele protsessidele.
Rakendused ja olulisus
Keemiline kineetika on oluline paljudes valdkondades: reaktsioonide optimeerimine keemiatööstuses, keskkonnaprotsesside modelleerimine (näiteks õhu saaste lagunemine), farmaatsiatoodete süntees, materiaalseadmete vananemine ja biokineetika. Mõistes reaktsiooni kiirust ja mehhanismi saab vähendada energiat kasutamist, parandada saagisid ja suurendada ohutust protsessides.
Kokkuvõtlikult võimaldab keemiline kineetika selgitada, miks ja kuidas reaktsioonid toimuvad erinevate tingimuste all, kuidas neid kontrollida ja kuidas leida optimaalseid tingimusi nii teadusuuringutes kui ka tööstuslikes rakendustes.