NS1-reaktsioon on asendusreaktsioon orgaanilises keemias. "SN" tähistab nukleofiilset asendust ja "1" tähistab asjaolu, et kiirust määrav samm hõlmab ainult ühte molekuli (unimolekulaarne). Reaktsioon kulgeb tavaliselt läbi karbokatsiooni kui vaheühendi. Anorgaaniliste keemikute seas tuntakse NS1-reaktsiooni sageli dissotsiatiivse mehhanismina. Christopher Ingold jt pakkusid selle reaktsioonimehhanismi esmakordselt välja 1940. aastal.
Mehhanism
SN1-mehhanism on kahest etapist koosnev:
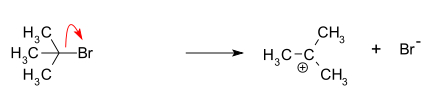
- 1) Lahustuva rühma lahutus (lahkumine) — substraat (näiteks alküülhalogeniid või protonitud alkohol) kaotab leaving-grupi, moodustades karbokatsiooni. See samm on aeglasem ja seega kiirust määrav samm.
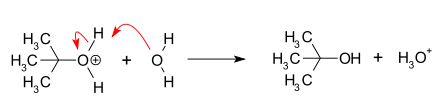
- 2) Nukleofiili lähenemine — vaba karbokatsioonile lisandub nukleofiil, moodustades lõpptoodangu.
Kuna kiirust määrav on ainult esimene samm, sõltub reaktsiooni kiirus ainult lähteaines oleva substradi kontsentratsioonist: rate = k[substrate]. Nukleofiili kontsentratsioon ei mõjuta kiirust oluliselt.
Faktorid, mis SN1-i soodustavad
- Karbokatsiooni stabiilsus: tertsiaarsed > sekundaarsed > primaarsed. Erinevad stabiliseerivad tegurid (induktne toime, hulgeneerimine, resonants) suurendavad SN1-liikumise tõenäosust.
- Resonantsi stabiilsus: bensüül- ja allyyl-substradid võivad SN1-reaktsioonis käituda kergemini, kuna karbokatsioonid on resonantsstabiilsed.
- Hea leaving‑grupp: tugevad leaving‑rühmad (nt halogeniidid, water pärast protoneerimist) soodustavad dissotsiatsiooni.
- Polaarne, protistaatne solvent: lahustid, mis stabiliseerivad ioone (nt vesi, alkoholid), soodustavad karbokatsiooni tekke ja seega SN1‑teed.
- Madalam nukleofiili tugevus: tugevad aluselised nukleofiilid eelistavad tihti bimolekulaarset NS2-reaktsiooni, mistõttu nõrgem-kuumem nukleofiil koos polaarse protistaatse keskkonnaga soosib SN1-i.
- Happelised tingimused alkoholide korral: alkohole tuleb esmalt protonida, et muuta –OH paremaks leaving‑grupiks; seetõttu kulgevad alkoholide asendused sageli happelises meediumis.
Stereokeemia ja vaheühendid
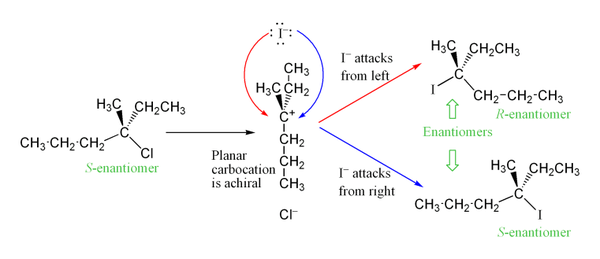
Kuna keskne karbokatsioon on sp2‑hübriidiseeritud ja plaaniline, võib nukleofiil lisanduda kahele poole võrdselt — seetõttu on oodata enamikul juhtudel otse racemise (racemise) tekke optiliselt aktiivsetest lähteainetest. Praktikas võib aga täheldada osalist säilimist või inverntsiooni, kui karbokatsiooni ja lahkuva rühma vahel on intiimne ionipaar (ion pair), mis piirab nukleofiili ligipääsu ühele küljelt.
Reaktsioonide näited ja rakendused
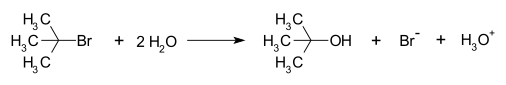
- Terts‑butüülkloriidi hüdrolüüs vees: t‑BuCl + H2O → t‑BuOH (solvolüüs), kus esineb SN1‑mehhanism ning kiirus sõltub ainult t‑BuCl kontsentratsioonist.
- Bensüül- ja allyülsubstradid: sekundaarsed bensüül‑ või allyül‑halogeniidid võivad SN1‑iga käituda kergemini kui tüüpilised primaarsed alkiilid, kuna karbokatsioon on resonantsiga stabiliseeritud.
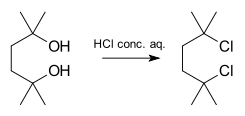
- Alkoholide asendused happelistes tingimustes: alkoholi protonimine ja järgneva vee lahkumine moodustab karbokatsiooni, millele järgneb nukleofiilne lisandumine.
Spetsiifilised ilmingud ja erandid
Rearrangeerumised: sageli toimuvad 1,2‑hydride või alküül‑nihked, kui tekkinud karbokatsioon suudab ümber järjestada end stabiilsema karbokatsiooni suunas (näiteks 2° → 3°), mis muudab saadused ootamatuks võrreldes lihtsa asendusega.
Naudingud keemilises sünteesis: SN1‑teed kasutatakse teadlikult siis, kui soovitakse kasutada resonantsstabiilseid või tertsiaarseid keskkondi ning kui nukleofiilina on lahusti ise (solvolüüs) või nõrk nukleofiil.
Tõendid ja ajalugu
SN1‑mehhanismi toe andsid kiirust määravad eksperimendid, karbokatsioonide tuvastamine ja reagendid, mis karbokatsioone tabavad (trapping), samuti sõltuvus lahusti polaarsusest ja leaving‑rühma paremuse mõjust kiirusele. Nagu mainitud, oli selle mehhanismi algne kirjeldus Christopher Ingoldi ja kolleegide töö tulemus 1940. aastatel (reaktsioonimehhanism).
Kokkuvõtlikult: SN1 on unimolekulaarne nukleofiilne asendus, mida iseloomustab karbokatsiooni vaheühendi teke, kiiruse sõltumine ainult substradist, soodustamine polaarsetes protistaatsetes lahustites ning kalduvus racemise ja rearrangeerumiste poole. Primaarsete alküülhalogeniidide puhul on tavaline alternatiiv NS2-reaktsioon.