SN 2 reaktsioon (tuntud ka kui bimolekulaarne nukleofiilne asendamine) on orgaanilise keemia asendusreaktsioon. See on nukleofiilse asendamise tüüp, kus nukleofiili üksikpaar ründab elektronpuudulikku elektrofiilset keskust ja seob end sellega. See tõrjub välja teise rühma, mida nimetatakse "lahkuvaks rühmaks". Seega asendab sissetulev rühm lahkuva rühma ühe sammuga. Kuna reaktsiooni aeglases, kiirust määravas etapis on kaasatud kaks reageerivat liiki, siis on sellest tekkinud nimetus bimolekulaarne nukleofiilne asendamine ehk SN 2. Anorgaaniliste keemikute seas tuntakse SN 2 reaktsiooni sageli vahetusmehhanismina.
Mehhanism ja üleminekuolek
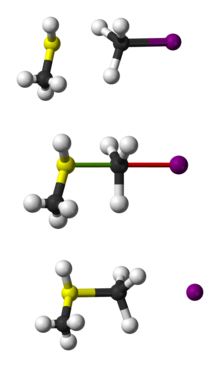
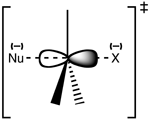
SN 2 toimub ühe sammuna: nukleofiil ründab substratsiooni elektrofiilset süsinikku otse vastassuunast (nn backside attack), samal ajal lahkub lahkuv rühm. Reaktsiooni üleminekuolek on korrapäratu pentakoordinaatne struktuur (osaline negatiivne laeng nii nukleofiilil kui ka lahkuval rühmal), mille korral sideme teke ja katkestamine toimuvad samaaegselt ilma eraldi vaheühendita.
Kineetika
SN 2 kineetika on teine järku: reaktsiooni kiirust määrab nii nukleofiili kui ka elektrooniliselt kahjustatud süsiniku kontsentratsioon. Kiiruseväljend:
- rate = k [substraat] [nukleofiil]
See tähendab, et kiirus muutub proportsionaalselt mõlema reageendi kontsentratsioonidega.
Stereokeemia
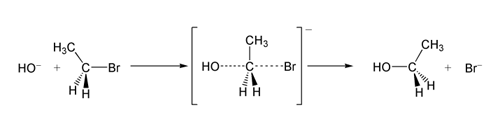
Tavaliselt SN 2 põhjustab Waldeni inversiooni — kui asendatav süsinik on stereoakesk, siis toimub konfiguratsiooni pöördumine (nt R → S). See on otsene tagajärg nukleofiili tagaajamisele ja tagumise rünnaku geomeetriale.
Mõjuvad tegurid
- Substraadi tüüp: SN 2 on kiireim primaarsetel ja metüülsetel süsinikel, aeglasem sekundaarsetel ning praktiliselt võimatu tertsiaarsetel — steriline takistus takistab backside attack'i.
- Nukleofiili tugevus: tugevam (rohkem laenguga või vähem delokaliseeritud) nukleofiil kiirendab SN 2. Negatiivsed ioonid (nt OH-, RS-) on tavaliselt tugevamad nukleofiilid kui neutraalsed molekulid.
- Lahkuva rühma kvaliteet: hea lahkuv rühm (nt I-, Br-, tosülaat) stabiliseerib lahkumisel saadavat laengut ja soodustab SN 2.
- Solvent: polar aprotic (nt DMSO, DMF, acetone) soodustavad SN 2, sest nad ei sidu tugevalt nukleofiile; protic (nt vee ja alkoholid) solvendid hääldavad tugevalt anioone H-sidemetega, nõrgendades nukleofiilide reaktiivsust.
- Temperatuur ja kontsentratsioon: kõrgem temp ja suuremad kontsentratsioonid kiirendavad üldiselt reaktsiooni.
Praktilised näited ja rakendused
- Methüülbromiid + OH- → metanol — lihtne metüül-substitutsiooni näide, mis kulgeb SN 2 teel.
- Alkoksüde (RO-) asendamine alküülsulfaadi või halogeniidiga, orgaanilises sünteesis kasutatavad funktsioonivahetused.
- SN 2 on lahutamatu osa paljudest sünteetilistest strateegiatest, näiteks heterotsüklite moodustamisel või kätteviimise astmel aktsepteeritud funktsionaalsuste asendamisel.
Võrdlus SN 2 vs SN 1 ja E2
- SN 1: toimub kaheastmelise mehhanismiga ja jälgib esimest järku kineetikat; SN 1 soodustub tertsiaarsetel süsinikel ja protic solventides; annab segatud stereokeemia (racemise) juhul, kui vaheühend on karbokatioon.
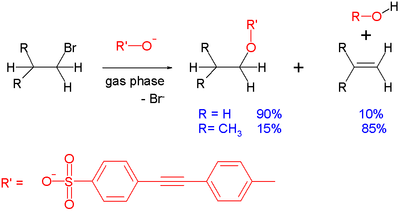
- E2: bimolekulaarne elimineerimine, samuti second-order kineetikaga; tihti konkureerib SN 2-ga, eriti sekundaarsete substratide ja tugevate basi/reaktiivsete nukleofiilide puhul; viimase korral tähtis on ka happe alfa-protoonide kättesaadavus ja geomeetriline nõue (anti-periplanaarne orientatsioon).
Energia- ja tööriistade märkused
SN 2-l on üks hästi defineeritud üleminekuolekule vastav energiatõus; reaktsiooni kiirus ja valikulisus sõltuvad ühestelt termodünaamilistest ja kineetilistest parameetritest (laengute stabiliseerimine, solvendi mõju, hüpoteetilised lahkuvate rühmade pKa-d jms). Reaktsioone modelleeritakse tihti DFT- või mehaanilise analüüsiga, et hinnata üleminekuolekuid ja energiabarjääre.
Kokkuvõte
SN 2 on lihtne, aga laialdaselt oluline orgaanilise keemia mehhanism, mille eripärad — bimolekulaarsus, teisest järku kineetika, backside attack ja Waldeni inversioon — määravad paljude sünteesistrateegiate valikulisuse ja efektiivsuse. Reaktsiooni edukus sõltub substraadist, nukleofiilist, lahkuvast rühmast ja solventist ning sageli tuleb arvestada konkurentsi teiste mehhanismidega nagu SN 1 ja E2.