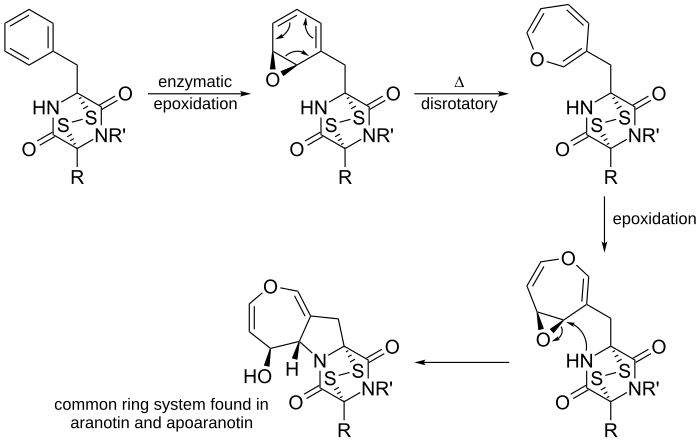
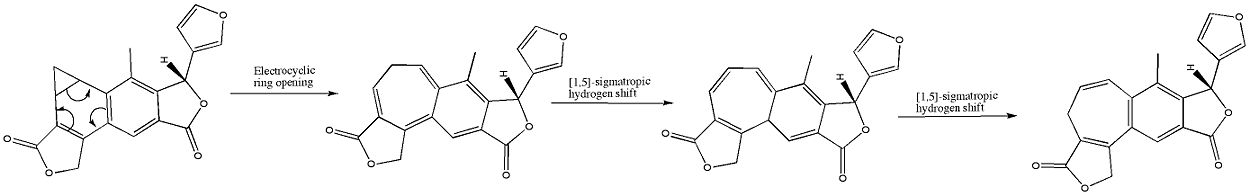
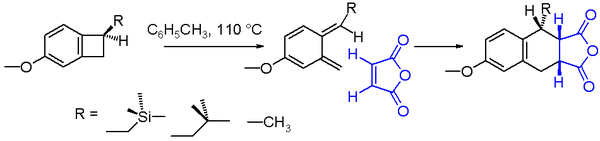
Orgaanilises keemias on elektrotsükliline reaktsioon üks peritsüklilise ümberpaiknemise reaktsiooni tüüp. Reaktsioon on elektrotsükliline, kui tulemuseks on, et üks pi-side muutub üheks sigma-sidemeks või üks sigma-side muutub pi-sidemeks. Elektrotsüklilistel reaktsioonidel on järgmised omadused:
- elektrotsüklilised reaktsioonid toimuvad valguse (fotoindutseeritud) või soojuse (termilise) toimel.
- reaktsioonirežiimi määrab pi-elektronide arv selles osas, kus on rohkem pi-sidemeid
- elektrotsükliline reaktsioon võib sulgeda rõnga (elektrotsükliseerimine) või avada rõnga.
- stereospetsiifilisus on määratud konrotatoorse või disrotatoorse üleminekuseisundi moodustumisega, nagu on ette nähtud Woodward-Hoffmanni reeglitega.
Woodward–Hoffmanni reeglid ja elektronide arv
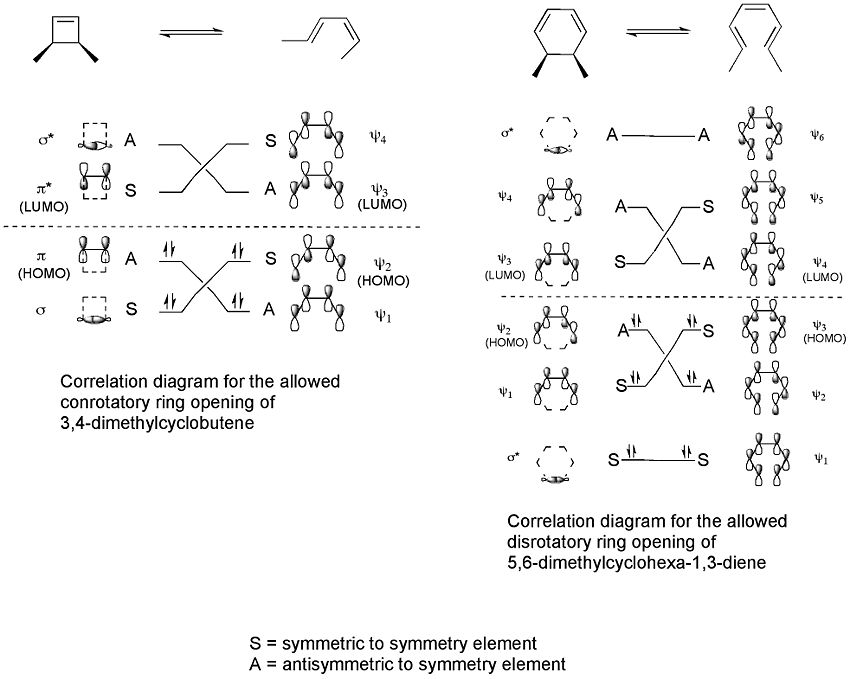
Woodward–Hoffmanni reeglid ennustavad, milline üleminekuseisund (konrotatoorne või disrotatoorne) on sümboolse reaktsiooni käigus sümmeetriliselt lubatud, lähtudes pi-orbitaalide sümmeetria säilimisest. Lihtsustatult kehtib reegel:
- Termiliselt: süsteemid, millel on (4n + 2) π-elektroni, läbivad disrotatoorse elektrotsüklilise protsessi; süsteemid, millel on 4n π-elektroni, läbivad konrotatoorse protsessi.
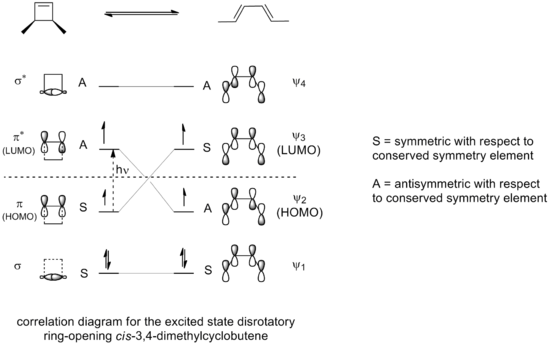
- Fotokeemiliselt on see käitumine ümberpööratud: (4n + 2) süsteemid → konrotatoorsed, 4n süsteemid → disrotatoorsed.
See tuleneb molekuliorbitaalide täitmisest ja HOMO (kõrgeima hõivatud molekuliorbitaali) sümmeetriast nii alg- kui ka lõppoleku suhtes.
Meehanism: serva-orbitaalide (frontier orbital) lähenemine
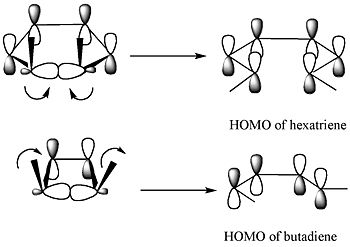
Piiri-orbiidi ehk frontiera-orbitaali meetod selgitab, kuidas elektrotsüklilised reaktsioonid toimivad. Reaktsiooni ajal peab tekkivate p-orbitaalide faas ja sümmeetria sobituma produkti vastava HOMO-ga. Näiteks sigma-sidet lõhkudes tekivad avatud otstes p-orbitaalid, mis peavad olema sama faasi- ja sümmeetriapoolse järjestusega kui butadieeni HOMO. Kui sobiv sümmeetria on võimalik ainult konrotatsiooniga, siis konrotatsiooniline rada on kiirem ja stereospetsiifiline tulemus järgneb sellele rajale.
Stereokeemia ja torquoselektiivsus
Torquoselektiivsus viitab sellele, kummal pool ja millises suunas substituendid ringi avanemise või sulgemise ajal pöörlevad. Teoreetiliselt võib konrotatsiooni puhul substituent pöörduda kas kella- või vastupäeva suunas; kui mõlemad pöörded on võrdselt tõenäolised, tekib racemaatiline segu seonduvatest stereoisomeeridest. Torquoselektiivses reaktsioonis on üks pöörlemissuund eelistatud (osaliselt või täielikult), mis viib ühe enantiomeeri ülekaaluni.
Torquoselektiivsuse põhjused:
- sterilised efektid (suured substituendid eelistavad pöörata eemale vastastikustest takistustest);
- elektroonilised efektid (elektronirikkad või -vaesed rühmad mõjutavad orbitaalide energiat);
- koordineerimine katalüsaatoriga (nt Lewis-happed võivad muuta orbitaalide energiaid ja suunata pöörlemist);
- lahusti- ja temperatuuriefektid ning lähtegrupi konformatsioon.
Näited ja praktikaline tähendus
Üks tuntud näide on 3,4-dimetüültsüklobuteeni termiline ring-avamisreaktsioon, kus cis-isomeer annab ainult cis,trans-2,4-heksadieeni, samas kui trans-isomeer annab trans,trans-2,4-heksadieeni. Selle stereospetsiifilisuse põhjuseks on konrotatsiooniline rõnga avanemine antud 4-π-süsteemi puhul ja substituentide pöördumise mustrid:
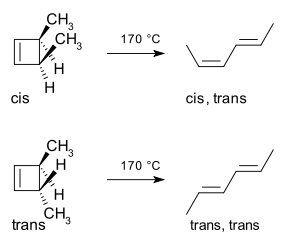
Joonisel on näha, kuidas sigma-side avanemise järgsed p-orbitaalid vastavad butadieeni HOMO sümmeetriale; ainult konrotatsiooniline ava- või sulgemismehhanism annab sobiva faasiühtluse. Selle selgitamiseks kasutatakse sageli järgmisi samme:
- määra reaktsioonis osalevate π-elektronide arv;
- rakenda Woodward–Hoffmanni reegleid, et ennustada konrotatoorset või disrotatoorset rada termilisel või fotokeemilisel tingimusel;
- kontrolli substituentide ja katalüsaatori mõjusid torquoselektiivsuse osas;
- katse- ja arvutuslikud andmed (NMR, röntgendifraktsioon, DFT-arvutused) kinnitavad ideaaljuhul ennustusi.
Nazarovi tsükilisatsioon ja teised spetsiifilised näited
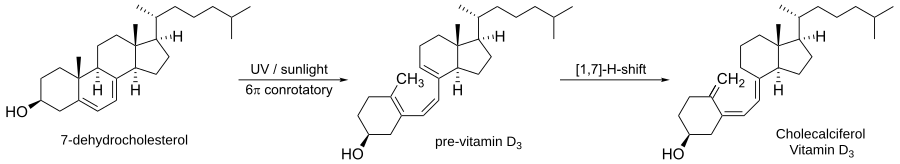
Keemikud on huvitatud elektrotsüklilistest reaktsioonidest, sest molekulide geomeetria kinnitab mitmeid teoreetiliste keemikute poolt tehtud ennustusi ja näitab orbitaalide sümmeetriasäilimist. Nazarovi tsüklilisatsioonireaktsioon on klassikaline näide elektrotsüklilisest tsüklisatsioonist: see sulgeb tsükli, muutes divinüülketoonid tsüklopenteenoonideks (see protsess toimib sageli happekatalüüsi all). Nazarovi tsüklisatsioon on tegelikult 4-π elektrotsükliline sulgemine (4n elektroni näide), mis termilisel tingimusel käib konrotatoorselt.
Põhjalikumad kommentaarid ja eksperimentaalne kontroll
Elektrotsüklilise reaktsiooni mekanismi ja stereospetsiifilisuse kontrollimiseks kasutatakse mitmeid meetodeid:
- termilise vs fotokeemilise tingimuse võrdlemine, et testida orbitaalsümmeetria mõju;
- substituentide varieerimine ja katalüsaatorite (nt Lewis-happede) lisamine torquoselektiivsuse uurimiseks;
- spektrilised meetodid (1H, 13C NMR, IR) ning kristallograafia lõpptoodete stereokeemia määramiseks;
- teoreetilised arvutused (MO- ja DFT-analüüs), et modelleerida HOMO/LUMO faasi ja neile vastavaid üleminekuseisundeid.
Kokkuvõte
Elektrotsüklilised reaktsioonid on peritsükliliste ümbersuunamiste alamklass, mille puhul toimub sigma- ja pi-sidemete vahel kõikumine vastavalt orbitaalide sümmeetriale. Woodward–Hoffmanni reeglid, frontiera-orbitaali analüüs ja torquoselektiivsus annavad vahendid, millega ennustada ja juhtida nende reaktsioonide stereokeemiat nii laboris kui sünteetilises orgaanilises keemias. Praktikas võimaldavad need reaktsioonid moodustada tsükleid või avada neid stereospetsiifilisel viisil, mis on oluline keerukate molekulide sünteesis.
Üheks näiteks on 3,4-dimetüültsüklobuteeni termiline ring-avamisreaktsioon. Cis-isomeer annab ainult cis,trans-2,4-heksadieeni. Trans-isomeer annab aga trans,trans-dieeni:
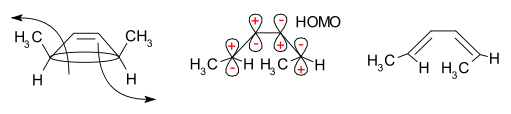
Tulemuse stereospetsiifilisus sõltub sellest, kas reaktsioon kulgeb konrotatoorse või disrotatoorse protsessi kaudu ning millised steriilsed ja elektroonilised mõjud juhivad torquoselektiivsust.