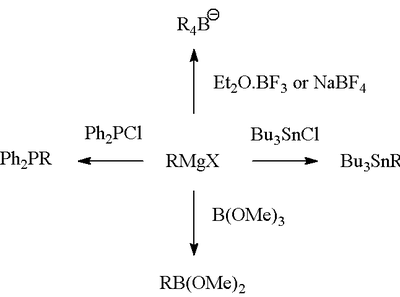
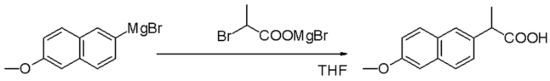
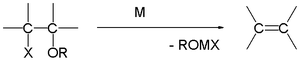
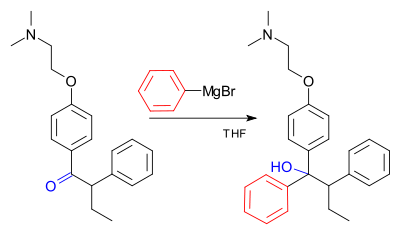
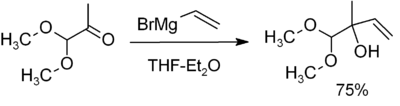Grignardi reaktsioon (hääldatakse /ɡriɲar/) on metallorgaaniline keemiline reaktsioon, mille käigus alküül‑ või arüül‑magneesiumhalogeniidid (Grignardi reaktiivid) tekivad magneesiumi ja orgaanilise halogeniidi reaktsioonil ning seejärel ründavad polaarsetes sidemetes olevaid elektrofiilseid süsinikuaatomeid (näiteks karbonüülrühmas). Grignardi reaktiivid toimivad nukleofiilidena ja on väga tõhus vahend uute süsinik‑süsinik sidemete moodustamiseks. Lisaks süsinik‑süsinik sidemetele võib Grignardi reaktsioon anda ka süsinik‑heteroatoomisidemeid (nt C–B, C–Si, C–Sn jt).
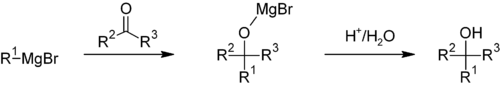
Kuidas Grignardi reaktiiv moodustub
Grignardi reaktiivid valmistatakse üldjuhul halogeenitud orgaanilisest ühendist (R–X, kus X = Cl, Br, I) reageerimisel magneesiumiga kuivades eeterlahustites (näiteks dieter või eetris, tihti kasutatakse ka THF‑i). Lihtsustatud üldväljend moodustumiseks:
R–X + Mg → R–MgX
Reaktsioon algab magneesiumi pinnal toimuva elektroniedastusega, mis võib anda lühiajalisi radikaalseid vaheühendeid ning lõppkokkuvõttes viia orgaanilise aniooni‑laadse R‑rühma sidumisele magneesiumiga. Tekkinud R–MgX esineb lahuses sageli agregaatidena või kompleksidena, mida stabiliseerivad eetermolekulid.
Mehhanism (lühike kirjeldus)
- Initsieerimine: magneesiumi pind annab elektroni halogeenitud orgaanilisele ühendiile, tekitades radikaalseid või anionseid vaheühendeid.
- Formatsioon: radikaalid ja halogeniidid kombineeruvad/muunduvad, moodustades organomagneesiumühendi R–MgX.
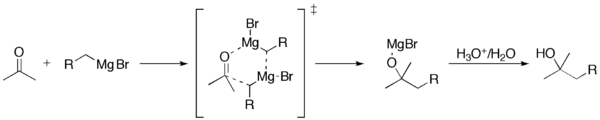
- Nukleofiilne lisandumine: moodustunud Grignardi reaktiiv ründab elektrofiilset keskonda (nt karbonüülrühma), andes magneesiumiga seotud alkoksaadi (magnesiumalkoksaat).
- Hüdrolüüs (vahetus): reaktsiooni lõpetamisel lisatakse hapet (nt vesilahus), mis protoneerib alkoksaadi ja annab lõpliku alkoholi või muu prootonitud produkti.
Mõnel juhul võib reaktsiooni algus ja edasised sammud toimida ka läbi üksikute elektroniedastuste (radikaalsetena), sõltuvalt reaktandite iseloomust ja tingimustest.
Tüüpilised reaktsioonid ja reaktsioonitüübid
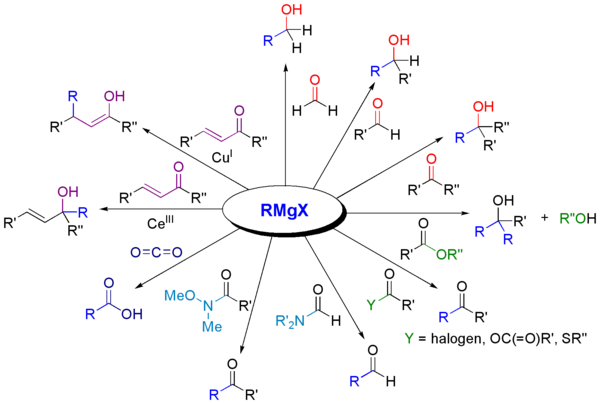
- Lisandumine karbonüülühenditele: aldehüüdid ja ketoonid → vastavalt primaarseid, sekundaarseid või tertiaarseid alkohole pärast hüdrolüüsi (nt formaldehüüd → primaarne alkohol; ketoon → tertiaalne alkohol).
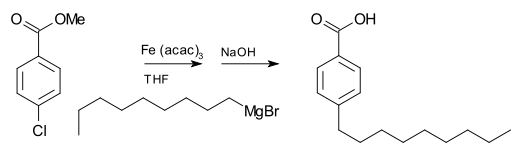
- Reaktsioon süsihappegaasi (CO2) puhul: R–MgX + CO2 → R–COOMgX → (happelise töötluse järel) R–COOH (karboksüülhape).
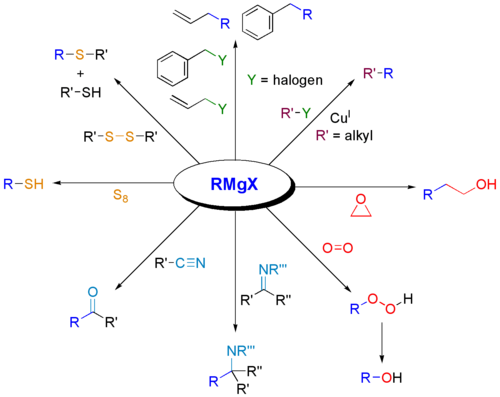
- Epossükkli avamine: Grignardi ründab epoksiide regiosele avamisele, andes alkoholi, mille külge on uus süsinikrühm lisandunud.
- Estritega reageerimine: tavaliselt toimub kahekordne lisandumine (esimene lisandumine annab ketooni vaheühendi, teine lisandumine annab tertiaarse alkoholi).
- Transmetallatsioon ja edasised funktsionaalsemaks kasutamiseks sobivad reaktsioonid (nt cross‑coupling eelkäijana või lähteühendina).
Tingimused ja praktiline käsitlus
Grignardi reaktsioonid nõuavad niiskusevabu tingimusi — happelised prootonid või vesi hävitavad reaktiivi, kuna R–MgX reageerib kiirelt prootoniga ja annab RH (alkaan) ning magneesiumhüdroksiidi. Seetõttu kasutatakse tavaliselt inertset atmosfääri (lämmastik, argon), leekkuivatatud klaasnõusid ja kuiva lahustit. Üks levinumaid lahusteid on dieter või THF, kuna need stabiliseerivad R–MgX koordineerudes magneesiumile.
Praktilised meetmed niiskuse vältimiseks:
- klaasnõude leekkuivatamine või ahjus kuivatamine;
- reaktsioonide läbiviimine anoodse inertse gaasi all (N2 või Ar);
- lahuste ja reagentide eelkuivatamine (molekulaarjaod, destilleerimine);
- magneesiumi aktiveerimine (nt ioodi lisamine, ultraheli, mehaaniline hõõrumine või kasutamine Rieke‑Mg‑sarnaseid väga aktiivseid vorme), et alustada reaktsiooni ja parandada saagisid.
Piirangud ja ohud
Grignardi reaktiivide peamised puudused ja piirangud:
- Reaktiivsus protise (prootoniga) seotud rühmadega — neid ei saa tavaliselt kasutada ühendis, mis sisaldab vabasid alkoholide, amiinide, karboksüülhapete või muude happeliste prootonite rühmi.
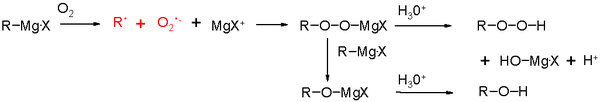
- Hapniku ja niiskuse tundlikkus — isegi väike kogus vett või õhuniiskust võib reaktsiooni saagiseid oluliselt vähendada.
- Halogeniidi tüüp mõjutab moodustumise kergust: tavaliselt on reaktiivsuse järjekord RI > RBr > RCl (R–F praktiliselt ei reageeri). Mõned arüül‑ ja vinüülkloriidid on raskemini reaktiivsed ja vajavad aktiivsemaid tingimusi.
- Grignardi reaktiivid ei moodusta lihtsalt C–C sidet SN2‑mehhanismiga alküülhalogeniididega; selle asemel toimub reaktiivide moodustumise etapil pigem keerukam mehhanism ja otsene SN2 vaheliste reaktsioonide kaudu C–C sidemete loomine ei ole tavaline tee.
- Õhus ja vees võivad Grignardi reaktiivid süttida või põhjustada ohtlikke kõrvalreaktsioone; töö käigus tuleb järgida laboritäpsust ja ohutusjuhiseid.
Keemilised modifikatsioonid ja alternatiivid
Juhul kui otse Grignardi reaktiive kasutada ei saa, kasutatakse sageli alternatiive või muudetud lähenemisi: organolithium ühendid (nt n‑BuLi) on tugevamad nukleofiilid ja baas, Rieke‑metallid (aktiivsed magneesiumivormid) või orgaaniliste magneesiumühendite preparaadid, mis on valmistatud spetsiaalsetes tingimustes. Ka ligandi‑abistatud Grignardi (nt TMEDA‑ga) või polaarsemates lahustes võivad käituda erinevalt ja võimaldada hankida raskemini ligipääsetavaid reaktiive.
Rakendused
Grignardi reaktsioon on keemias äärmiselt väärtuslik sünteetiline vahend. Peamised rakendused:
- uute C–C sidemete loomine orgaanilises sünteesis (farmaatsia, looduslike ühendite süntees, orgaanilised materjalid);
- alkoholide ja karboksüülhapete tootmine (sõltuvalt quenchist);
- mitmesuguste funktsionaalsete rühmade omastamine (nt epoksiidide avamine, estrite ja nitrilidega töötlemine teatud tingimustel);
- Grignardi reaktiivid on olnud sünteesi tööhobuse staatuses ja neid nimetatakse sageli „esmasteks lihasteks“ orgaanilises sünteesis—lihtsa reageerimisvõime tõttu on võimalik kiiresti lisada alifaatseid või aromaatseid fragmente keerukatesse molekulidesse.
Ajalooline taust
Avastaja oli prantsuse keemik François Auguste Victor Grignard, kelle töö Grignardi reagentide ja reaktsioonide väljatöötamisel tõi talle 1912. aastal Nobeli keemiapreemia. Tema töö võimaldas senisest oluliselt lihtsamalt ja usaldusväärsemalt luua uusi süsinik‑süsinik sidemeid, mis muutis orgaanilise keemia sünteetilisi võimalusi.
Kokkuvõttes on Grignardi reaktsioon universaalne ja laialdaselt kasutatav meetod orgaanilises sünteesis, kuid selle praktiline kasutamine nõuab hoolikat kuivust ja inertset keskkonda ning teadmisi reagendi piirangute kohta.