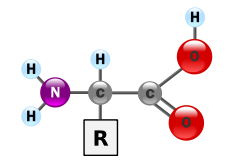
Aminohapped on valkude ehitusplokid. Eukarüootidel on 20 standardset aminohapet, millest valmistatakse peaaegu kõik valgud.
Biokeemias on aminohape mis tahes molekul, millel on nii amiini (NH2+R) kui ka karboksüül (C=O) funktsionaalsed rühmad. Biokeemias tähistab see mõiste alfa-aminohappeid üldvalemiga H2NCHRCOOH, kus R on üks paljudest külgrühmadest (vt joonis).
Teada on umbes 500 aminohapet. Loomade jaoks on aminohapete tähtsaim ülesanne luua valke, mis on väga pikad aminohapete ahelad. Igal valgul on oma aminohapete järjestus ja see järjestus muudab valgud erineva kujuga ja erineva funktsiooniga. Aminohapped on nagu valkude tähestik; kuigi sul on ainult mõned tähed, saad neid ühendades teha palju erinevaid lauseid.
Üheksa standardset aminohapet 20-st on inimese jaoks "hädavajalikud" aminohapped. Inimese organism ei saa neid ehitada (sünteesida) teistest ühenditest ja seega tuleb neid võtta toiduga. Teised võivad olla hädavajalikud teatud vanuses või haigusseisundites. Vajalikud aminohapped võivad ka liigiti erineda. Taimtoidulistel loomadel on vaja saada asendamatuid aminohappeid oma toidust, mis mõnede puhul on peaaegu täielikult rohi. Mäletsejalised, näiteks lehmad, saavad osa aminohappeid mikroobide kaudu kahes esimeses maokambris.
Struktuur ja keemilised omadused
Aminohape koosneb tavaliselt kolmest iseloomulikust osast: amino(-NH2) rühmast, karboksüül(-COOH) rühmast ja külgrühmast (R), mis määrab aminohappe keemilised omadused. Enamik bioloogiliselt tähtsaid aminohappeid on alfa-aminohapped, kus amino- ja karboksüülrühmad on seotud sama süsinikuaatomiga (H2NCHRCOOH,).
Paljud aminohapped eksisteerivad vesilahuses zweetairioonidena (mõlemad grupid osaliselt laenguga), mistõttu neil on konkreetne pKa väärtus nii amino- kui ka karboksüülrühmale. Mõned külgrühmad on laetud (happelised või aluselised), teised polaarsed või mittepolaarsed — see määrab aminohappe käitumise valgus ja lahustes.
Aminohapped on ka ketruseliigsed (kiraalsed) — enamikel standardsetel aminohapetel (välja arvatud glütsiin) on asümmeetriline alfa-süsinik, mis annab L- ja D- vormid; enamik kasutatavaid keerdesid organismides on L-vormid.
Tüübid ja klassifikatsioon
- Standardseid (genetiliselt kodeeritud) aminohappeid: eukarüootidel see rühm sisaldab 20 tavalisemat aminohapet, mida kodeerib universaalne geenikood ja kasutatakse valkude sünteesiks.
- Mitteeetandardseid või modifitseeritud aminohappeid: raku sees esinevad ka teised aminohapped (näiteks hüdroksüproliin, dimetüülarginiin), mis tekivad post-translationaalsete modifikatsioonide käigus või ei kuulu tavalisele 20 hulka.
- Asendamatud (hädavajalikud) aminohapped: need, mida organism ei suuda ise sünteesida ja tuleb saada toidust. Inimesel on neid tavaliselt üheksa (nt leutsiin, valiin, lüsiin jt), kuid täpne arv võib sõltuda vanusest ja seisundist.
- Asendatavad: organism saab neid ise sünteesida teistest ainetest (nt glutamiin, alaniin).
- Hästi tingimuslikult asendatavad: need võivad olla tähtsad teatud perioodidel (imetamise ajal, haigus, kasv) — näiteks arginiin võib olla noorloomadele tingimuslikult asendamatu.
Roll valkude sünteesis (translatsioon)
Valgud sünteesitakse rakkudes informatsiooni põhjal, mis on kodeeritud DNA-s ja vahendatud mRNA kaudu. Peamised sammud:
- Transkriptsioon: DNA info kopeeritakse mRNA‑ks.
- tRNA ja aminoatsüül-tRNA süntees: iga aminohape seotakse vastava tRNA molekuliga aminoatsüül-tRNA‑syntetatsaasi abil. See „laadib“ tRNA õige aminohappega.
- Translatsioon ribosoomis: ribosoom loeb mRNA kolme nukleotiidi kaupa (kodon) ja toob vastava aminoatsüül-tRNA. Ribosoom katalüüsib peptiidsideme tekkimist aminohapete vahel, moodustades kasvava polüpeptiidahela.
- Peptiidside: tekib amino- ja karboksüülrühma vahel kondenseerumise teel, vabastades veemolekuli.
Valgude lõplik 3D‑struktuur (primaar-, sekundaar-, terciaal- ja kvaternaarstruktuur) sõltub aminohapete järjestusest ning külgrühmade keemilisest iseloomust. Õige voltimine on oluline funktsiooni tagamiseks.
Post-translationaalsed modificatsioonid ja funktsionaalne mitmekesisus
Pärast algset sünteesi võivad valkudes toimuma mitmed keemilised muudatused: fosforüülimine, atsetüülimine, glükosüülimine, tsüstiinide disulfiidsillad jm. Need muutused võivad muuta valgu aktiivsust, paiknemist rakus või stabiilsust.
Süntees ja ainevahetus
Mitte kõik aminohapped sünteesitakse ühtemoodi — mõned tekivad lihtsate modifikatsioonide teel muudest aminohapetest või metaboliseeritakse süsivesikutest ja lämmastikust. Keskmine ainevahetus hõlmab transaminaasi reaktsioone, dekarboksüülimist ja teisi samme, mis on seotud lämmastiku ringlusega (nt uureatsükkel).
Toitumine, allikad ja tähendus tervisele
Aminohapete tasakaal toidus on eluliselt tähtis. Täisväärtuslikud valgud (nt liha, kala, muna, piimatooted, mõned soja‑ ja tseerealised kombinatsioonid) sisaldavad kõiki asendamatuid aminohappeid. Taimse toidu tarbimisel on oluline kombineerida erinevaid valguallikaid, et saada vajalik kogus kõiki asendamatuid aminohappeid.
Aminohapete puudus võib põhjustada kasvupeetust, immuunsüsteemi nõrgenemist ja muid ainevahetushäireid. Liigne vaba aminohapete tarbimine võib samuti koormata maks ja neerusid ning mõjutada ainevahetust.
Rakendused ja teaduslik tähtsus
- Meditsiin: aminohapete tasakaalu ja üksikute aminohapete lisandid kasutatakse teatud haiguste raviks või taastusravis (nt fenüülketonuuria, maksahaigused, traumajärgne taastumine).
- Toidulisandid ja sport: üksikud aminohapped või BCAA segud on populaarsed lihasmassi ja taastumise toetamiseks.
- Biotehnoloogia: aminohapete teadmised on alus valkude disainiks, ravimite loomiseks ja sünteetiliste ainete tootmiseks.
Kokkuvõte
Aminohapped on bioloogiliselt üliolulised molekulid — nii valkude ehitusplokid kui ka metaboolsed vahendajad. Nende keemiline mitmekesisus ja roll translatsioonis annavad organismidele suure funktsionaalse paindlikkuse. Õige aminohapete mitmekesisus toidus ja rakkude võime neid reguleerida on tervise ja kasvu jaoks hädavajalik.