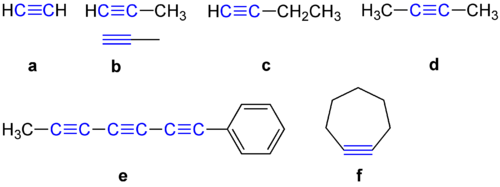
Alküün on molekul, millel on kahe süsinikuaatomi vahel kolmikside. Alküünide üldvalem on CnH2n-2. Neid nimetatakse ka atsetüleenideks; väikseim alküün on atsetüleen (etüün). Alküünid on hüdrofoobsed: nad on hästi lahustuvad orgaanilistes lahustites, kuid halvasti vees.
Struktuur ja füüsikalised omadused
Alküünide kolmiksideme puhul on süsiniku aatomid sp-hübriidiseerunud, mis annab sidemele lineaarse geomeetria ja 180° nurga aatomite vahel. Kolmikside sisaldab ühte σ- ja kahte π-sidet, mis mõjutab nii sideme tugevust kui ka reaktiivsust. Väiksemad alküünid (nt C2–C4) on toatemperatuuril gaasilised, pikemad ahelad on vedelad või tahked sõltuvalt ahelapikkusest.
Keemilised omadused ja reaktiivsus
Alküünid on tavalisest süsivesinikust reaktiivsemad ja paljudes reaktsioonides sageli reaktiivsemad ka kui alkeenid. Erinevalt alkaanidest on alküünidel kättesaadavad π-electronid, mis osalevad lisamisreaktsioonides.
Terminalsetel alküünidel (kus kolmikside asub ahela lõpus) on prootoneid suhteliselt happelised (pKa ≈ 25) ning neid on võimalik eemaldada tugeva alusega (näiteks NaNH2 või n-BuLi). Tekkinud alküülide anioone (atsetüüliidid) kasutatakse laialdaselt liitumisreaktsioonides ja süsiniku-süsiniku sideme moodustamisel — näiteks lisamisel ketoonile või alküülhalogeniidile (alküülimine).
Lisamisreaktsioonid: alküünid undergo additsiooni, näiteks halogeenimine, hüdrohalogenimine ja hidratsioon. Hidratsioon happega ja Hg(II)-katalüüsiga annab tavaliselt ketooni (enooltautomeerumine), samas kui hydroboration-oxidation terminalset alküüni oksüdeerib sageli aldehüüdi (antimarkovnikovi käitumine pärast oksüdeerimist).
Redutseerimine: alküünid on suhteliselt kergesti redutseeritavad kaksiksidemeks. Osaline hüdrogenatsioon Lindlari katalüsaatoriga annab cis-alkeeni, samas kui lahustunud metalli (nt Na/NH3) vähendamine annab tavaliselt trans-alkeeni. Täielik hüdrogenatsioon viib alkaanini.
Oksüdeerimine ja lõhustumine: tugeva oksüdeerija (nt KMnO4, O3) toimel lõhustatakse kolmiksidemeid, tulemuseks võivad olla karboksüülhapped (terminalse alküüni puhul karboksüülhape ja karboksüülhape lõikes olevatest aatomitest) või ketoonid, sõltuvalt substituentidest.
Peritsüklilised ja katalüütilised reaktsioonid: alküünid osalevad mitmesugustes peritsüklilistes reaktsioonides, sealhulgas tsüklotrimereerimistes ja 1,3-dipolaarsetes tsüklisaadditionides (näiteks atsiidi-alküüni 1,3-dipolaartses tsüklisünteesis — nn “click chemistry” puhul). Lisaks on alküünid olulised metallkatalüüsitud ühendamisreaktsioonides (nt Sonogashira-koupling Csp–Csp2 sidemete moodustamiseks).
Klassifikatsioon ja kasutus
- Terminalsed alküünid — kolmikside ahela lõpus; võimaldavad deprotonatsiooni ja alküülimist.
- Internalsed alküünid — kolmikside ahela keskel; tavaliselt vähem happelised ja mõnevõrra vähem reaktiivsed deprotonatsiooni suhtes.
Praktiliselt kasutatakse alküüne orgaanilises sünteesis süsinik-süsiniku sidemete moodustamiseks, heterotsükliliste ühendite sünteesiks, materjaliteaduses (nt konjugeeritud süsteemides) ning tööstuslikes protsessides (nt polümeeride või eri-funktsionaalsete vaheühendite süntees). Tänu oma reaktiivsusele ja mitmekülgsele sünteetilisele rakendatavusele on alküünid tähtsad reagendid kaasaegses orgaanilises keemias.